2012
5
Autores:
Marcelo Rodríguez G.1, 2, José Antonio Moreno S.1, 2, Alejandro Soto A.2, Rolando Márquez A2, Ricardo Eltit V.3
Instituciones:
1Departamento de Obstetricia y Ginecología, Escuela de Medicina, Universidad de Valparaíso, 2Unidad de Medicina Materno Fetal,.
Tipo de documento:
Casos ClínicosMIOCARDITIS Y BLOQUEO AURÍCULO-VENTRICULAR FETAL ASOCIADO A LUPUS ERITEMATOSO SISTÉMICO MATERNO
Contenido del documento:
RESUMEN
El lupus eritematoso sistémico (LES) es una de las patologías autoinmunes más frecuentes durante el embarazo, asociándose con distintas complicaciones fetales y neonatales, sobre todo cardíacas, secundario al traspaso de anticuerpos maternos a través de la placenta. Estos anticuerpos se unen a los cardiomiocitos fetales, desencadenando una respuesta inflamatoria local que determina la aparición de lesiones que pueden ser permanentes y letales. Presentamos el caso de una paciente embarazada con LES, en la cual se observó en el feto la presencia de bloqueo aurículo-ventricular de primer grado y signos sugerentes de miocarditis. Estas complicaciones se caracterizan por un aumento en la morbimortalidad perinatal, por lo que las estrategias actuales están dirigidas a la detección precoz de éstas y también en la prevención de las mismas. Un tratamiento estándar aun es tema de investigación, pese a los reportes que muestran la efectividad de corticoides como la dexametasona. En embarazadas con anticuerpos anti-Ro positivo se recomienda efectuar ecocardiograma fetal seriados cada 1-2 semanas desde la semana 16, para detectar precozmente anomalías cardiacas sobre las cuales pudiese intervenirse.
PALABRAS CLAVE: Lupus eritematoso sistémico, lupus neonatal, bloqueo aurículo-ventricular, anti-Ro, anti-La
SUMMARY
Systemic lupus erythematosus (SLE) is one of the most common autoimmune disease during pregnancy, associated with various fetal and neonatal complications, especially heart disease, secondary to the transfer of maternal antibodies through the placenta. These antibodies bind to fetal cardiomyocytes, triggering a local inflammatory response that determines the appearance of lesions that may become permanent and deadly. We report a pregnant patient with SLE, in which was observed the presence of atrioventricular block of 1st degree and signs suggestive of myocarditis in the fetus. These complications are characterized by an increase in fetal and neonatal morbidity and mortality, so that current strategies are aimed at early detection of these and also in preventing them. A standard therapy for atrioventricular block is still matter of investigation, although corticosteroids like dexamethasone have been reported to be effective for associated cardiomyopathy. Serial echocardiograms and obstetric sonograms, performed at least every 1–2 weeks starting from the 16th week of gestational age, are recommended in anti-Ro/SSA-positive pregnant women to detect early fetal abnormalities that might be a target of preventive therapy.
KEY WORDS: Systemic lupus erythematosus, neonatal lupus, atrioventricular block, anti-Ro, anti-La
INTRODUCCIÓN
El embarazo asociado a Lupus Eritematoso Sistémico (LES) se relaciona con la aparición de complicaciones cardíacas en el feto, secundario al traspaso de anticuerpos maternos a través de la placenta (1). Estos anticuerpos se unen a los cardiomiocitos fetales, desencadenando una respuesta inflamatoria local que determina la aparición de lesiones que pueden ser permanentes y letales (2,3).
Presentamos el caso de una paciente embarazada con LES, en la cual se observó en el feto la presencia de bloqueo auriculo ventricular (BAV) de primer grado y signos sugerentes de miocarditis.
Caso clínico
Paciente de 29 años, multípara de 2 hijos sanos, con antecedente de LES inactivo sin tratamiento. En el embarazo actual inicia sus controles en el policlínico de alto riesgo obstétrico a las 26 semanas, indicándose exámenes generales de control prenatal e inmunológicos. No asiste a los controles, retomándolos a las 34 semanas.
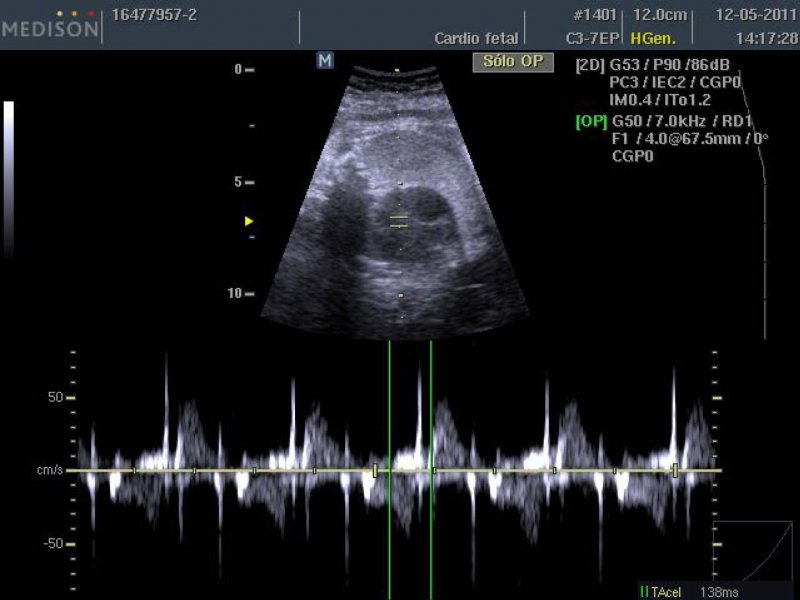
Los exámenes muestran anticuerpos anti-Ro de 37,3 U/ml y anti-La de 6 U/ml, parámetros hematológicos y de función renal normales. Se observa ecográficamente un feto de 1815 g, creciendo en percentil 15 de la curva MINSAL, con Doppler de arteria umbilical y cerebral media normales, y aumento del índice de pulsatilidad (IP >p 95) del ductus venoso. A la exploración cardíaca se observó una prolongación del intervalo PR mecánico (158 mseg) (Figura 1), una leve ecogenicidad en endocardio y válvula mitral, con un aumento del índice de función miocárdica (TEI index de 0,52) sugerente de disfunción ventricular. En el resto de la exploración anatómica destaca polihidroamnios (ILA 25 cm) y una bolsa gástrica pequeña. Los diagnósticos de ingreso fueron BAV de primer grado, miocarditis fetal, probable atresia esofágica con fístula traquoesofágica.
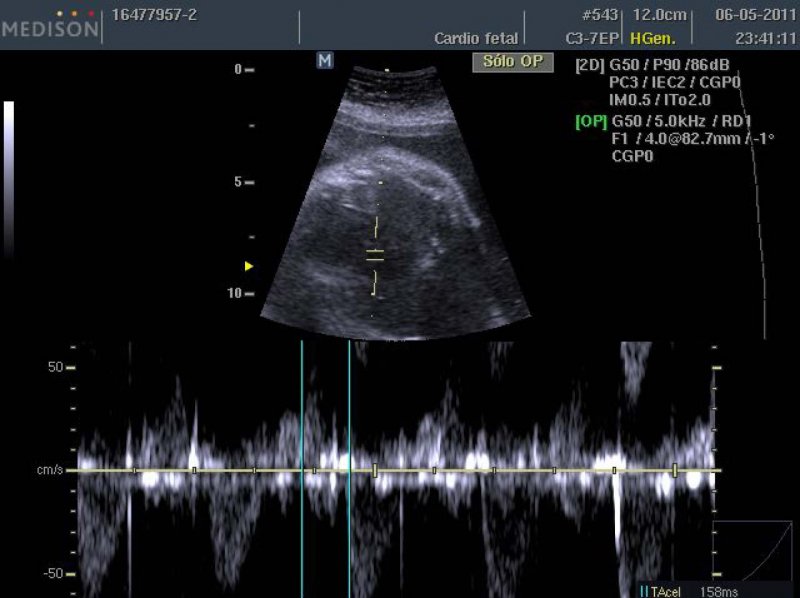
Se inicia tratamiento con dexametasona 4 mg/día, observándose normalización del intervalo PR mecánico al sexto día de tratamiento (Figura 2). Respecto de la evaluación miocárdica, no se observa variación, persistiendo un IP de ductus venoso >p95 y un índice de función miocárdica alterado.
Se decide la interrupción del embarazo a las 36 semanas, vía alta, obteniéndose un recién nacido de 2.690 g, confirmándose el diagnóstico de atresia esofágica, operado al día siguiente con evolución posoperatoria satisfactoria. La evaluación ecocardiográfica neonatal reveló ecogenicidad subendocárdica, con función miocárdica normal (Figura 3).
DISCUSIÓN
El lupus neonatal corresponde a un cuadro asociado a la presencia de anticuerpos maternos específicos, que se presenta en 1 cada 2000 recién nacidos vivos (1,4), que se caracteriza por la presencia de rash cutáneo, pancitopenia, disfunción hepática y compromiso cardiaco (5). Las manifestaciones cutáneas, hematológicas y hepáticas se resuelven dentro de pocos meses, a medida que ocurre el clearence de anticuerpos. En cambio, las manifestaciones cardiológicas tienden a ser irreversibles, puesto que se asocian a la presencia de un daño permanente en el tejido miocardico (6).
El compromiso cardíaco en el lupus neonatal puede ser de dos tipos, el BAV congénito y la miocardiopatía (7). Ambos están relacionados con el traspaso transplacentario de anticuerpos anti-Ro/anti-La, dirigidos hacia antígenos nucleares, y que a través de los procesos de apoptosis e inflamación producen el daño en la célula miocardica (8,9). Si bien inicialmente se pensaba que ambos anticuerpos estaban relacionados con las complicaciones cardíacas, evidencia reciente sostiene que sería la familia de anticuerpos anti Ro los responsables del daño, específicamente el polipéptido anti Ro 52- kDa (10,11).
Bloqueo aurículo-ventricular congénito. Corresponde a un disturbio en la conducción aurículo-ventricular. Existen de primer, segundo y tercer grado, siendo este último el más severo y característicamente asociado a la presencia de anticuerpos en el plasma materno. Este bloqueo de tercer grado o BAV completo (BAVC) se caracteriza porque la comunicación eléctrica a través del nodo AV está interrumpida, por lo que la frecuencia cardíaca está determinada por el automatismo ventricular, que es mucho más lento que el auricular (12). Esta complicación se observa en 1-3% de los hijos de madres con anticuerpos anti-Ro/anti-La, con una recurrencia en el siguiente embarazo de 8-25%(13). La mortalidad asociada es de 18-43%. La aparición de este BAVC ocurre en general entre las 18- 24 semanas (14).
Desde el punto de vista fisiopatológico, el daño se produce principalmente por la acción del anticuerpo anti-Ro 52 KD, el cual se une a células miocárdicas induciendo apoptosis, ocurriendo posteriormente un reemplazo por tejido fibroso incapaz de transmitir el impulso eléctrico (9,15).
Respecto del manejo del BAVC, la estrategia más utilizada está dirigida a contrarrestar la inflamación mediante el uso de corticoides (16). Jaeggi y cols (14), utilizaron dexametasona y betamiméticos en 21 pacientes con BAVC, y observaron un 95% de nacidos vivos y 95% de sobrevida al año, comparado con 77% y 46% del grupo control. Pese a este aparente incremento en los resultados favorables, el BAVC sigue siendo una complicación grave, que condiciona un aumento importante en la morbimortalidad perinatal.
Por lo anterior, las estrategias actuales están orientadas a tratar a pacientes en riesgo de desarrollar BAVC, cuyos fetos presentan bloqueo de primer y segundo grado, entendiendo que probablemente estas condiciones se desarrollarían previamente a la aparición del BAVC, y que serían la evolución natural de éste.
La manera de pesquisar a las pacientes sería mediante la medición del intervalo PR mecánico, definiendo como bloqueo de primer grado a un intervalo PR >150 mseg (17). Esta técnica ha mostrado una buena correlación con el ECG fetal (18). El objetivo de la pesquisa precoz sería iniciar el tratamiento con corticoides, previniendo la progresión a BAVC. Una de las primeras experiencias fue la de Vesel y cols (19), quienes a una paciente con 25 semanas de embarazo, portadora de anticuerpos anti-Ro/anti-La, y en presencia de bloqueo de primer grado, iniciaron dexametasona 4 mg/día por 4 semanas, mostrando regresión de la prolongación del intervalo PR. En un estudio posterior (20), 6 pacientes con BAV de primer grado fueron tratadas con dexametasona, observándose normalización de la conducción AV dentro de 3 a 14 días. Dado el resultado de estos estudios, el tratamiento de los estadios iniciales del BAV con corticoides aparece como una estrategia interesante para prevenir el BAVC en pacientes con anticuerpos anti-Ro/anti-La.
Sin embargo, los resultados de estudios recientes ponen en duda la eficacia de esta estrategia. En éstos se ha observado que pacientes con BAV de primer grado y sin tratamiento no muestran progresión hacia BAVC, y que incluso pueden mostrar regresión espontánea durante el período neonatal (21). Además, se documentó que los fetos que desarrollaron BAVC lo hicieron de manera súbita, sin una prolongación previa del intervalo PR (22). De esta manera, se genera incertidumbre sobre la fisiopatología e historia natural del BAVC, en el cual posiblemente el daño se produce súbitamente, sin un BAV primer grado previo.
Miocarditis. Otra complicación observada en los fetos expuestos a anticuerpos anti-Ro/anti-La es el compromiso miocardico difuso, que puede presentarse con o sin BAV, e independiente del uso de marcapaso posnatal (23,24). Puede observarse en ecocardiografía pre y posnatal, mediante una serie de hallazgos, entre los que destaca dilatación ventricular, disfunción sistólica, hipertrofia miocardica y ecogenicidad del endocardio (25-28). Con respecto a este último, es el hallazgo más observado, y se asocia con fibroelastosis endocárdica, que corresponde a una fibrosis del tejido, y que desde el punto de vista fisiopatológico ocurre por un depósito masivo de inmunoglobulinas en el miocardio, desencadenando un proceso de inflamación, con la posterior hiperplasia de colágeno y elastina, generando un engrosamiento difuso del endocardio (23). El pronóstico en los casos de disfunción miocardica clínica y en ausencia de intervención es bastante pobre, con una mortalidad descrita sobre 80% (25,26).
En cuanto al manejo, se ha descrito el uso de corticoides, inmunoglobulinas endovenosas (IGIV) y plasmaferesis. Trucco y cols (29), en su estudio determinan que la utilización de corticoides e IGIV en fetos con diagnóstico de miocardiopatía y fibroelastosis endocárdica aparentemente mejoraría los resultados.
En el caso clínico presentado, la paciente era portadora de un LES, con niveles de anticuerpos anti-Ro de 37,3 U/ml, y si bien presentó alteración de la conducción AV, ésta sólo fue de primer grado. Esto es concordante con los reportes que señalan que el riesgo de desarrollar BAVC es de sólo un 1-3% de los casos, y que este riesgo se ha observado únicamente con niveles de anticuerpos anti-Ro >50 U/ml (30). Además presentó ecogenicidad endocárdica, lo que asociado a alteración del ductus venoso y del Índice de Función Miocárdica, indican la presencia de una fibroelastosis endocardica asociada a una disfunción miocardica. El tratamiento prenatal se asoció con una regresión del BAV de primer grado, tal como ha sido reportado por otras publicaciones, pero sin una normalización prenatal de los parámetros funcionales del miocardio. Pese a esto, la evolución posnatal desde el punto de vista miocardico fue adecuada, con una evaluación ecocardiográfica dentro de límites normales.
CONCLUSIÓN
El LES materno se asocia con la presencia de autoanticuerpos capaces de atravesar la placenta y producir lesiones específicas a nivel del miocardio fetal, tales como BAVC y miocarditis. Estas complicaciones se caracterizan por un aumento evidente en la morbimortalidad fetal y neonatal, por lo que las estrategias actuales están dirigidas a la detección precoz y prevención de las mismas.
BIBLIOGRAFÍA
1. Silverman ED, Laxer RM. Neonatal lupus erythematosus. Pediatr Rheum 1997;23:599-618.
2. Weston WL, Harmon C, Peebles C, et al. A serological marker for neonatal lupus. Br J Dermatol 1982;107:377-82.
3. Scott JS, Maddison PJ, Taylor PV, et al. Connective-tissue disease, antibodies to ribonucleoprotein, and congenital heart block. N Engl J Med 1983;309:209-12.
4. Cimaz RG, Spence D, Hornberger LK, Silverman ED. Defining the incidence and spectrum of neonatal lupus erythematosus: a prospective study of infants born to mothers with anti-Ro autoantibodies. J Pediatr 2003;142:678-83.
5. Buyon JP, Ben-Chetrit E, Karp S, et al. Acquired congenital heart block. Pattern of maternal antibody response to biochemically defined antigens of the SSA/Ro-SSB/La system in neonatal lupus. J Clin Invest 1989;84:627-34.
6. Buyon J, Clancy R, Friedman D. Cardiac manifestations of neonatal lupus erythematosus: guidelines to management, integrating clues from the bench and beside. Rheumatology 2009;5:139-48.
7. Hornberger LK, Al Rajja N. Spectrum of cardiac involvement in neonatal lupus. Scand J Immunol 2010;72:189-97.
8. Boutjdir M. Serum and IgG from the mother of a child with congenital heart block induce conduction abnormalities and inhibit L-type calcium channels in a rat heart model. Pediatr Res 1998;80:354-62.
9. Clancy RM, Askanase AD, Kapur RP, et al. Impaired clearance of apoptotic cardiocytes linked to anti-SSA/Ro-SSB/La antibodies in pathogenesis of congenital heart block. J Clin Invest 2006;116:2413-22.
10. Defendenti C, Atzeni F, Spina M, et al. Clinical and laboratory aspects of Ro/SSA-52 autoantibodies. Autoimmunity Rev 2011;10:150-4.
11. Buyon JP, Ben-Chetrit E, Karp S, et al. Acquired congenital heart block. Pattern of maternal antibody response to biochemically defined antigens of the SSA/Ro-SSB/La system in neonatal lupus. J Clin Invest 1989;84:627-34.
12. Jaeggi E, Friedberg M. Diagnosis and management of fetal bradyarrhythmias. Pacing Clin Electrophyisiol 2008;31 suppl 1:s50-3.
13. Llanos C, Izmirly PM, Kartholi M, et al. Recurrence rates of cardiac manifestations associated with neonatal lupus and maternal/fetal risk factors. Arthritis Rheum 2009;60:3091-7.
14. Jaeggi ET, Hamilton RM, Silverman ED, et al. Outcome of children with fetal neonatal childhood diagnosis of isolated complete heart block. A single institution`s experience. J Am Coll Cardiol 2002;39:130-7.
15. Clancy RM, Kapur RP, Molad Y, et al. Immunohistologic evidence supports apoptosis, IgG deposition and novel macrophage/fibroblast crosstalk in the pathologic cascade leading to congenital heart block. Arthritis Rheum 2004;50:173-82.
16. Brucato A. Prevenction of congenital heart block in children of SSA-positive mothers. Rheumathology 2088;47:35-7.
17. Pasquini L, Seale A, Belmar C, et al. PR interval: a comparision of electrical and mechanical methods in the fetus. Early Human Develop 2007;83:231-7.
18. Bergman G, Wahren-Herlenius M, Sonesson S-E. Diagnostic precision of Doppler flow echocardiography in fetus at risk for atrioventricular block. Ultrasound Obstet Gynecol 2010;36:561-6.
19. Vesel S, Mazic U, Blejec T, Podnar T. First degree heart block in the fetus of an Anti-SSA/Ro-positive mother. Arthritis Rheum 2004;50:2223-6.
20. Rein A, Mevorach D, Perles Z, et al. Early diagnosis and treatment of atroventricular block in the fetus exposed to maternal Anti-SSA/Ro-SSB/La antibodies: a prospective, observational, fetal kinetocardiogram-based study. Circulation 2009;119:1867-72.
21. Jaeggi E, Silverman E, Lskin C, et al. Prolonged of the atrioventricular conduction in fetus exposed to maternal Anti-Ro/SSA an Anti-La/SSB antibodies did not progressive heart block. J Am Coll Cardiol 2011;57:1487-92.
22. Friedman D, Kim M, Copel J, et al. Utility of cardiac monitoring in fetuses at risk for congenital heart block. The PR interval and dexamethasone evaluation (PRIDE) prospective study. Circulation 2008;117:485-93.
23. Nield L, Silverman E, Smallhorn J, et al. Endocardial fibroelastosis associated with maternal anti-Ro an anti-La antinodies in the absence of atrioventricular block. J Am Coll Cardiol 2002;40:796-802.
24. Costedoat-Chalumeau, Amoura Z, Villain E, et al. Anti-SSA/Ro antibodies and the heart: more than complete congebital heart block? A review of electrocardiographic and myocardial abnormalities and of treatment options. Arthritis Res Ther 2005;7:69-73.
25. Nield L, Silverman E, Taylor G, et al. Maternal anti-Ro and anti-La antibody-associated endocardial fibroelastosis. Circulation 2002;105:843-8.
26. Moak J, Barron K, Hougen T, et al. Congenital heart block: development of late-onset cardiomyopathy, a previously underappreciated sequela. J Am Coll Cardiol 2001;37:238-42.
27. Vaysse C, Touboul C, Kessler S, et al. Fetal myocarditis without congenital heart block. Prenat Diagn 2011;31:608-9.
28. Villeon C, Dulac Y, Ohanessian G, et al. Fetal myocarditis associated with maternal anti-Ro and anti-La antibodies in the absence of atrioventricular block with good outcome. Arch Pediatr 2010;17:1445-7.
29. Trucco S, Jaeggi E, Cuneo B, et al. Use of intravenous gamma globulin and corticosteroids in the treatment of maternal autoantibody-mediated cardiomyopathy. J Am Coll Cardiol 2011;57:715-23.
30. Jaeggi E, Laskin C, Hamilton R, et al. The importance of the level of maternal Anti-Ro/SSA antibodies as the prognostic marker of the development of cardiac neonatal lupus erythematosus. J Am Coll Cardiol 2010;55:2778-84.