2021
1
Autores:
Sochog
Instituciones:
Mariam Abulhaj Martínez (1), Águeda Bataller Calatayud(1), Salvador Selfa Moreno(2), Ana Viegas Sainz(1), Neus Garrido Molla(1), Antonio Vicente Antolí Francés(1).
1_ Unidad de gestión clínica de Obstetricía y Ginecología.
2_ Unidad de gestión clínica de Radiología. Hospital Lluís Alcanyís de Xátiva, Valencia, España.
Correspondencia: Mariam Abulhaj Martínez correo electrónico: abulhaj_mar@gva.es
Tipo de documento:
Casos ClínicosA propósito de un caso: Presentación atípica de rotura uterina
Contenido del documento:
INTRODUCCIÓN
La rotura completa es la disrupción de todas las capas de la pared uterina, incluyendo la serosa, por lo que hay comunicación directa con la cavidad abdominal, lo que conlleva una importante morbimortalidad materno-fetal. A diferencia de la dehiscencia que resulta en la disrupción incompleta sin repercusión clínica materno-fetal y cuyo diagnóstico suele realizarse casualmente en el momento de la cesárea.1
La cesárea anterior constituye actualmente el principal factor de riesgo para rotura, dado que se trata de una intervención quirúrgica previa que daña la integridad del miometrio incrementando la placentación anómala (placenta previa y acretismo placentario) y la disrupción uterina.1
En países desarrollados la primera causa es el intento de parto vaginal tras cesárea anterior, mientras que en países en vías de desarrollo es el estancamiento del expulsivo con imposibilidad de parto instrumental.2,3
Una de las causas que favorecen la rotura uterina es la inducción de parto en aquellas pacientes con cesárea previa respecto a las que inician el parto de forma espontánea (1,5% de riesgo en inducción respecto al 0,8 % con parto espontáneo); sin embargo, la incidencia varía según el método de inducción. El riesgo de rotura con inducción con misoprostol es bastante alto (2,45%) por lo que el American College de ginecología y obstetricia ha contraindicado su uso, pero los datos de rotura con el uso de otras prostangandinas son limitados. Respecto a la inducción con oxitocina el riesgo de rotura es levemente mayor (alrededor de un 1.1%) por lo que la mayoría de expertos no contraindican su uso en inducciones con cesárea previa.1
Además, existen otras circunstancias que podrían favorecer la rotura uterina, aunque su relación no está clara y, por tanto, no son especialmente útiles a la hora de predecir la posibilidad de rotura: edad materna avanzada, edad gestacional avanzada, peso fetal estimado de más de 4000g, intervalo entre partos menor de 18 -24 meses e histerorrafia en una capa. Los signos y síntomas que nos harían sospechar de rotura uterina anteparto o intraparto son: registro cardiotopográfico fetal anormal, dolor abdominal, sangrado vaginal, hematuria, inestabilidad hemodinámica materna, y dinámica uterina aumentada con pérdida de tono uterino. En el postparto el dolor abdominal y sangrado vaginal persistente que no cesa a pesar de diversos tratamientos uterotónicos serían sugerentes de rotura uterina.4,5
Para el diagnóstico de rotura uterina no se usan las pruebas de imagen de forma habitual, pues se trata de una emergencia obstétrica cuyo diagnóstico suele ser clínico. Si las condiciones fetales y maternas son estables y se sospecha una rotura, se puede utilizar una evaluación focalizada con ecografía u otro método de imagen que pueden mostrar uno o más de los siguientes signos: hemoperitoneo, rotura del miometrio, hematoma adyacente a la cicatriz de histerotomía, membranas fetales distendidas por líquido extrauterina, líquido peritoneal libre, anhidramnios, útero vacío, partes fetales fuera del útero y / o muerte fetal. La tomografía computarizada o la resonancia magnética realizadas como parte de una evaluación de traumatismos pueden detectar aire peritoneal, así como patologías asociadas con la rotura, como íleo y abscesos.1
En el caso que presentamos la rotura uterina no manifestó ninguno de estos signos ni síntomas; sino que debutó con fiebre puerperal cinco días después del parto En la bibliografía revisada no hemos encontrado ningún caso clínico de rotura uterina contenida por el sistema de coagulación, en el que pacientese mantuviera asintomática al alta hospitalaria y debutara posteriormente con fiebre puerperal y gran malestar general. De ahí la importancia del caso clínico que se describe, cuya relevancia radica en la importancia de instaurar un tratamiento precoz ante un diagnóstico inusual. Este caso clínico constituye un reto para los profesionales sanitarios a la hora de establecer un diagnóstico y tratamiento correctos. La demora del tratamiento o el tratamiento inadecuado puede finalizar en histerectomía, lesiones genito-urinarias, shock séptico e incluso la muerte materna.6 De modo que se presenta este caso clínico de rara aparición de rotura uterina; con el objetivo de revisar la literatura científica publicada respecto a los factores de riesgo, el diagnóstico y el tratamiento.
CASO CLÍNICO
Paciente de 28 años con antecedentes obstétricos de un aborto y una cesárea previa en el año 2013, atendida en el hospital Lluís Alcanyís de Játiva (Valencia, España). Embarazo previo de curso normal que se finaliza en semana 41 mediante prostanglandinas intravaginales por embarazo en vías de prolongación. Tras 4 horas con la misma exploración de 4cm se realiza una cesárea segmentaria transversa por no progresión del parto que cursa sin incidencias.
La gestación actual cursa de forma normoevolutiva, con terminación de la misma en semana 41 también por embarazo en vías de prolongación. La inducción del parto en este embarazo es con oxitocina. Tras 3 horas de inicio de la inducción se procede a aplicar la anestesia epidural y a las 5 horas de trabajo de parto se alcanza la dilatación completa. Finalización del parto mediante vacuo-metálico por expulsivo prolongado. Se aplica el vacuo-metálico en III plano de Hodge en la posición occipito iliaca izquierda anterior fetal y tras dos tracciones nace un recién nacido con APGAR 10/10, pH arterial 6,96 y peso 3920 gramos. Posteriormente se procede a la sutura de la episiotomía según práctica habitual. Durante el postparto presenta una cantidad de sangrado normal con el útero bien contraído. El puerperio inmediato cursa con anemia moderada (hemoglobina 8,4 g/dl; hematocrito 25,6%) con buena tolerancia y evolución. Al alta hospitalaria en la exploración el tacto vaginal es normal sin ningún hallazgo patológico, la episiotomía se encuentra en buen estado y los loquios son de aspecto y cantidad normal.
Cinco días post-parto la paciente acude a urgencias por fiebre de un día de evolución con una temperatura máxima en su domicilio de 39ºC, gran malestar general y dolor abdominal. A la exploración, la paciente presenta temperatura de 38,7ºC con puntos de episiotomía y loquios normales, abdomen doloroso a la palpación profunda en hipogastrio y tacto vaginal levemente doloroso a la movilización. En la ecografía abdominal y transvaginal se visualiza masa compleja (figura 1) de 10 x 6,7cm situada entre útero y vejiga compatible con gran coágulo (figura 2-3) que se continúa con cavidad endometrial y cérvix a través de un defecto completo de la pared lateral izquierda del cuello y cuerpo uterino (figura 4). Los hallazgos sugieren una rotura del cuello uterino y cicatriz uterina previa por lo que se decide ingreso para control del cuadro clínico y tratamiento quirúrgico.
Al ingreso se realiza hemograma que cursa con leucocitosis de 15,10 x 10 9/ L con desviación a la izquierda; hemoglobina de 10,2g/dl; hematocrito 30,4% y PCR de 127,1mg/L. Se instaura tratamiento antibiótico y analgésico intravenoso con augmentine 1g y enantyum cada 8 horas.
Se realiza laparotomía exploradora donde se visualiza gran hematoma en zona de histerorrafia de unos 11x7cm, que se extiende hasta parametrio derecho y hacia cavidad uterina por rotura uterina cervico-segmentaria de unos 5-6cm. Tras drenaje de hematoma y lavados de cavidad se realiza sutura por planos de rotura uterina a nivel segmentario hasta parametrio derecho. Se realiza mediante sutura continua con vycril del 0 en doble capa. Durante el post-operatorio se continúa con tratamiento antibiótico y analgésico con buena evolución clínica. La paciente se mantiene afebril con sangrado vaginal escaso por lo que se decide alta hospitalaria cinco días tras la intervención. Una semana después se cita en hospital de día para control, en la exploración se comprueba un abdomen blando y depresible, no doloroso; tacto vaginal anodino y loquios normales. En la ecografía trans-vaginal se visualiza útero regular, involucionado con línea endometrial de 3 mm, anejos normales, sin líquido libre en Douglas, ni hematoma en pared uterina.
DISCUSIÓN
La rotura uterina ocurre en 0,1% de todos los embarazos de término y se puede asociar a una dehiscencia de cicatriz uterina previa, un parto espontáneo rápido, estimulación excesiva con oxitocina, multiparidad, desproporción cefalopélvica o una presentación transversa no reconocida. Sin embargo, al existir el antecedente de una cesárea, aumenta a un 1%.7,8En una revisión sistemática en 2015 podemos encontrar que la incidencia de rotura uterina con cicatriz previa oscila entre 0,15-0,985 en trabajo de parto espontáneo, 0,3-1,5% en estimulación e inducción con oxitocina y 0,68-2,3% en inducciones con Prostaglandinas.9
En nuestro caso clínico se trata de una paciente con cesárea previa con inicio del parto mediante oxitocina y terminación del parto mediante vacuo-metálico, todos ellos factores de riesgo de la rotura.
La sospecha de rotura uterina debe estar presente cuando hay un desequilibrio entre tensión en la cicatriz y su fuerza. Según esta observación la rotura ocurre en la última parte de la fase activa o en la segunda etapa del trabajo de parto, cuando las presiones intrauterinas son mayores.10,11
Durante la rotura intraparto los síntomas que se describen son: dolor abdominal agudo, pérdida de bienestar fetal, pérdida del plano del feto, hemorragia vaginal y deterioro hemodinámico materno. Éstos signos y síntomas premonitorios de rotura uterina son muy llamativos en las pacientes sin cesárea anterior, pero en aquellas con cicatriz previa en ocasiones pueden pasar desapercibidos; de hecho, la clínica variará según el lugar de la rotura y el tipo de anestesia utilizada. Por ejemplo, una rotura en la parte posterior del útero o parametrios con anestesia epidural se manifiesta con grandes cambios en los signos vitales, pero mínimo dolor y sangrado de la paciente. Una rotura a nivel cervical se presentaría con abundante sangrado vaginal y la rotura sobreañadida de la vejiga debutaría con hematuria.12
En cuanto a la rotura postparto puede estar relacionado con la extracción fetal, un parto instrumental, alumbramiento manual, etc. Pudiendo aparecer las manifestaciones de forma tardía.3
La revisión uterina posparto es la exploración manual de la cavidad uterina que se realiza con el fin de detectar la presencia de restos placentarios, membranas ovulares y soluciones de continuidad en las paredes uterinas, que ha dejado de ser una técnica de rutina por exponer a las mujeres a mucho dolor y aumentar el riesgo de complicaciones de tipo infeccioso. Por tanto, la revisión manual de la cavidad uterina puede ayudar al diagnóstico precoz de disrupción de las paredes del útero como en el caso clínico expuesto, pero se debe limitar su indicación solo a aquellos casos con alta sospecha de rotura uterina.13
En el caso clínico que presentamos tanto la cicatriz previa como la anestesia podrían haber enmascarado parte de los síntomas característicos tras una disrupción completa de las capas de la pared uterina. Cabe pensar que lo más probable es que la rotura se hubiese producido tras el parto instrumental y dada su localización desde el segmento hasta el cérvix haber debutado con gran sangrado vaginal. Al haber quedado taponada la rotura por el gran hematoma no se presentó ningún signo ni síntoma propio de este cuadro clínico. En nuestro caso la manifestación tardía de dolor abdominal y poco habitual de fiebre puerperal cinco días postparto hizo pensar en un primer momento en una endometritis. De modo que la ecografía fue clave para poder establecer el diagnóstico definitivo. Tal y cómo hemos podido observar en las imágenes mostradas, el defecto completo de la pared uterina confirmaba la rotura que posteriormente fue confirmada mediante laparotomía exploradora.
En cuanto al procedimiento de histerectomía o reparación del defecto uterino se basa en la combinación de factores, incluyendo el deseo de la paciente para futuras gestaciones, la extensión de la rotura, la estabilidad hemodinámica intraoperatoria y las habilidades del cirujano para la consiguiente reparación. Si el defecto es reparado la bibliografía sugiere que es razonable realizarlo mediante aproximación de los bordes dañados, capa por capa con sutura reabsorbible, similar a la reparación de cualquier histerotomía.12
En nuestro caso clínico la reparación se realizó por planos suturando los bordes lacerados desde el nivel segmentario hasta el parametrio derecho mediante sutura continua en doble capa con vycril del 0.
Aunque no es obligatorio realizar ninguna medida de control antes del parto vaginal en caso de cesárea previa, actualmente hay que destacar que la medición ecográfica del grosor del segmento uterino o del grosor miometrial a nivel de la cicatriz de la cesárea anterior se ha propuesto como un factor predictor del riesgo de rotura uterina. A pesar de que existe una correlación entre menor grosor y mayor riesgo de rotura, no existe un punto de corte por debajo del cual se pueda contraindicar formalmente el parto vaginal. Un grosor de segmento uterino < 2mm se relaciona con un mayor riesgo de rotura. En caso de disponer de la información del grosor ecográfico puede utilizarse como un factor predictivo de mayor o menor riesgo de rotura uterina y tenerlo en cuenta en la toma de decisiones sobre la vía del parto, conjuntamente con la paciente.14
CONCLUSION
La incidencia de rotura uterina es muy baja por lo que el parto vaginal sigue siendo la vía de elección a pesar de presentar una cesárea anterior. La medición del segmento uterino previo parto puede ayudarnos a valorar el riesgo de rotura, aunque no existe un consenso sobre el punto de corte. Una vez se ha producido la complicación la sintomatología es clave para su diagnóstico, pero en aquellos casos con clínica atípica como el que presentamos , la ecografía puede ser clave para su diagnóstico precoz.
REFERENCIAS
- Landon MB, Heather F, Uterine rupture: After previous cesarean delivery. www.uptodate.com
- Oquendo CM, Beltrán MJ, Soriano OK. Rotura uterina espontánea en una paciente con polihidramnios como único factor de riesgo. Comunicación de un caso, revisión la bibliografía y experiencia institucional. Ginecol Obstet Mex 2008;76:217-220.
- Sociedad Española de Ginecología y Obstetricia. Protocolos SEGO: Rotura uterina. Prog Obstet Ginecol. 2015;58(6):296-299.
- Bustos P, Delgado J, Greibe D. Ruptura uterina espontánea por placenta percreta. Rev Chil Obstet Ginecol 2003;68:519-522.
- Chauhan SP, Martin JN Jr, Henrichs CE, Morrison JC, Magann EF National Institutes of Health Consensus Development Conference Panel.National Institutes of Health Consensus Development conference statement: vaginal birth after cesarean: new insights March 8-10, 2010. Obstet Gynecol 2010; 115:1279-95.
- Chauhan SP, Martin JN Jr, Henrichs CE, Morrison Jc, Magnan EF. Maternal and perinatal complications with uterine ruptura in 142,075 patients who attempted vaginal birth after cesarean delivery: A review of the literatura.
Am J Obstet Gynecol 2003; 189 (2):408-17.
- McMahon MJ, Luther ER, Bowes WA, Olshan AF: Comparison of a trial of labor with an elective second cesarean section. N Engl J Med 1996; 335: 689-95.
- Lydon-Rochelle M, Holt VL, Easterling TR, Martin DP: Risk of uterine rupture during labor among women with prior cesarean delivery. N Engl J Med 2001; 345: 38.
- Hidalgo Lopezosa P, Hidalgo Maestre M.Riesgo de rotura uterina en el parto vaginal tras cesárea revisión sistemática. Enfermeria Clinica, 2017; 27(1): 28-39.
- Hamilton EF, Bujold E, McNamara H, Gauthier R, Platt RW: Dystocia among women with symtomatic uterine rupture. Am J Obstet Gynecol 2001; 184: 620-4.
- Landon MB, Spong CY, Thom E, Hauth JC, Bloom SL, Varner MW, et al. Risk of uterine rupture with a trial of labor in women with multiple and single prior cesarean delivery. Obstet Gynecol. 2006;108:12–20.
- James F Smith, MD, MA Joseph R Wax, MD Uterine rupture: Unscarred uterus.uptodate.com
- Matthias Sachse-Aguilera,1 Omar Calvo-Aguilar. Indicaciones de la revisión manual de la cavidad uterina durante la tercera etapa de trabajo de parto. Revista CONAMED 2013, 18 (1):31-36
- Protocolo control gestacional en gestantes con cesárea anterior. Hospital Clínic. Hospital San Joan de Déu. Universitat de Barcelona.
FIGURAS
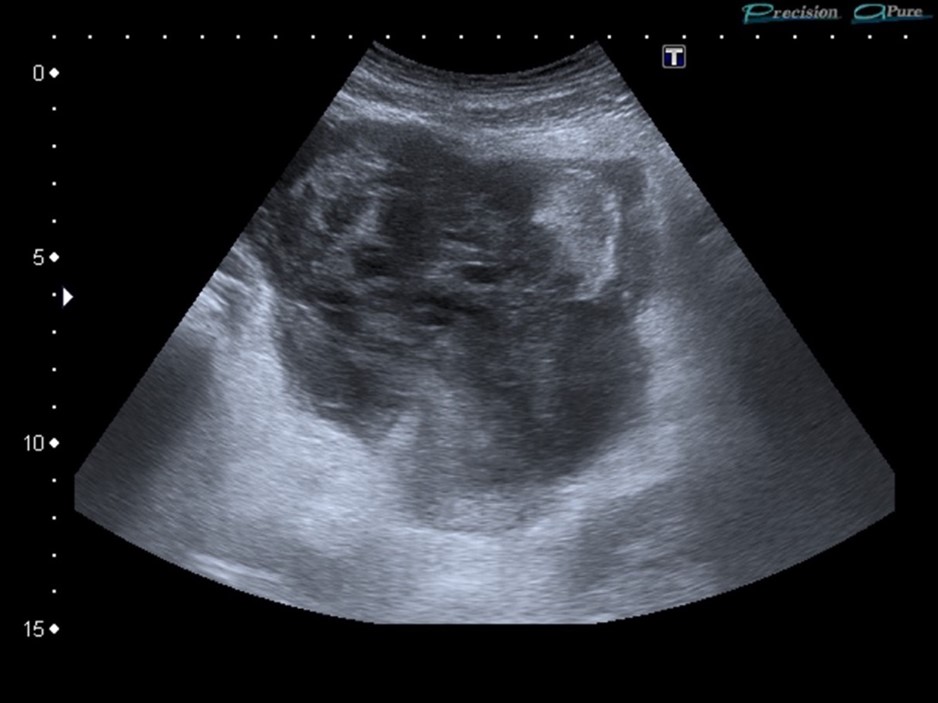
Figura 1. Masa compleja de 10 x6,7cm situada entre útero y vejiga compatible con gran coágulo.
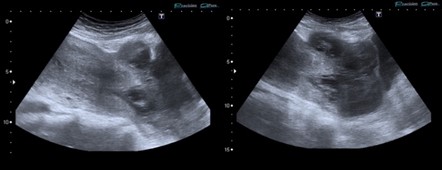
Figura 2 y 3. Gran coágulo que se continúa con cavidad endometrial y cérvix a través de un defecto completo de la pared lateral izquierda del cuello y cuerpo uterino correspondiente a una rotura del cuello uterino y cicatriz uterina previa.
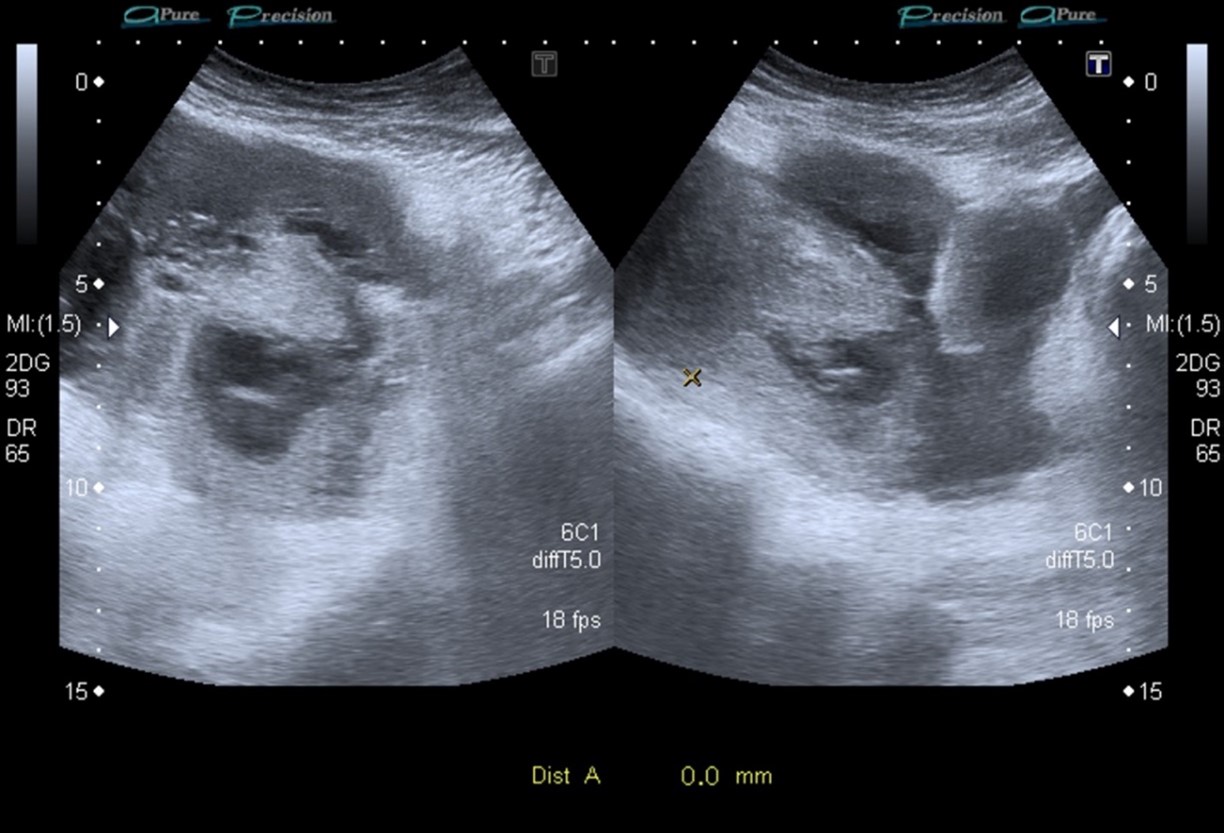
Figura 4. Defecto de pared uterina izquierda a nivel de histerorrafia previa.



