2020
4
Autores:
Brayan Alexander Rojas Mesa, Walter D. Cardona Maya.
Instituciones:
Grupo Reproducción, Departamento de Microbiología y Parasitología, Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia.
Tipo de documento:
Trabajos OriginalesEfecto de la borra de café sobre la biológica espermática: aproximación in vitro
Contenido del documento:
INTRODUCCIÓN
El café es un producto agrícola con importancia económica para muchos países, es así como para finales de 2018 se exportaron en el mundo más de 10 millones de sacos de café siendo Brasil, Colombia y Vietnam los tres principales exportadores 1. Esta alta exportación ratifica que la compra de café, con el propósito de ser usado como una bebida preparada mediante infusión a partir del fruto de los cafetos, se ha convertido en un elemento indispensable de la canasta familiar 2,3.
El fruto de café pertenece a la familia de las rubiáceas de las cuales existen 500 géneros y más de 6000 especies (el arábigo, la robusta, el liberiano y el excelso entre otras) 4, siendo las especies más importantes comercialmente el arábigo y la robusta. Todas las especies de café se caracterizan por tener más de 1000 sustancias químicas, incluyendo: carbohidratos, lípidos, compuestos nitrogenados, vitaminas, minerales, alcaloides además de compuestos fenólicos 3,5,6.
La robusta se caracteriza por tener el fruto de mayor concentración de cafeína, mientras que el fruto de la arábica presenta mayor producción y consumo en el mundo debido seguramente al aroma y suave sabor al paladar; sin ningún tratamiento el grano de café arábigo posee una concentración de cafeína relativamente bajo, entre 0,6 y 1,7% 6.
Durante la producción las semillas de café pasan por diferentes procesos de madurez, lavado, almacenamiento, selección y tostación antes de llegar a su presentación final como bebida. El proceso de tostación es fundamental y se basa en la transformación de los granos de café mediante la aplicación de calor generando cambios en el color, la forma, el volumen, la masa, la humedad y la densidad del grano induciendo variabilidad en las concentraciones de ácidos, proteínas, azúcares e incluso cafeína 7, modificando el olor y el sabor final del producto. En la industria cafetera uno de los residuos de mayor producción es la borra de café, representa el 10% del peso neto del café cosechado, contiene importantes cantidades de compuestos orgánicos como ácidos grasos, lignina, celulosa, hemicelulosa e incluso polisacáridos los cuales podrían explotarse como fuente de productos de valor agregado, incluyendo compostaje 8,9, producción de biodiesel, como fuente de azúcares, precursor para la producción de carbón, e incluso como bioabsorbentes de iones metálicos 10.
El compuesto más importante y reconocido del café es la cafeína, un estimulante del sistema nervioso central (SNC), con capacidad para aumentar las concentraciones de calcitonina, relajar los músculos lisos y estimular la frecuencia cardiaca 11; una ingesta moderada de 400 mg/día de cafeína no se asocia con ningún efecto adverso para la salud 12, solo las mujeres en edad reproductiva y los niños deberían tener restricciones para su consumo debido a que existe evidencia que demuestra que la ingesta de cafeína durante el primer trimestre del embarazo incrementa el riesgo de aborto espontáneo 12,13.
Durante los últimos 50 años el consumo de café se ha relacionado con diversos ámbitos de la salud debido a la popularidad y a los beneficios de su consumo, los efectos que puede generar en las personas que lo consumen constantemente se han asociado con la prevención de la diabetes mellitus tipo 2 (DM2) 14,15 y el riesgo cardiovascular 16,17. Sin embargo, el consumo de café moderado o alto se ha relacionado con un mayor riesgo de padecer carcinoma renal 18,19. En enfermedades como el Parkinson una taza de café al día se encuentra asociada a una reducción del 10% de riesgo a padecerla 20 y con respecto a la obesidad los extractos de café verde sugieren un beneficio al ser utilizados como suplementos para la reducción del peso 21,22.
Estos estudios que relacionan el café y la cafeína con afecciones como las enfermedades cardiovasculares 23-25, la DM2 26,27 y el cáncer 28 presentan resultados contradictorios 5,29 debido principalmente al tipo de café utilizado, además el consumo de café está estrechamente relacionado con otros factores de riesgo para estas enfermedades como el consumo de cigarrillo 18,20,30, la ingesta de alcohol 30 y el sedentarismo 31.
Desde otra perspectiva, durante los tratamientos de reproducción asistida en un estudio realizado sobre el impacto que genera la ingesta de café diaria en las mujeres danesas durante sus tratamientos de fertilidad, se demostró que entre una y cinco tazas de café por día, aumentan las probabilidades de obtener una resolución exitosa 32 y en el ámbito de la fertilidad masculina se evidencio que el consumo de más de 272 mg/día, está asociado a una menor probabilidad de concebir un bebe vivo 33. En contraste, existe evidencia sobre el efecto negativo del consumo de café sobre la fertilidad masculina 34 dada la característica que posee la cafeína de difundirse libremente en el ovario y los testículos humanos, esta propiedad fue descrita por Goldstein y Warren al evaluar testículos de pacientes sometidos a orquiectomía bilateral a causa del cáncer de próstata, a estos se les administró 1 g de benzoato sódico de cafeína 30 minutos antes del procedimiento quirúrgico, lo que posteriormente en la evaluación de los testículos mostró que la cafeína tiene acceso a las gónadas adultas y que logra en estos tejidos concentraciones similares a las del plasma 35.
De otro lado, el estrés oxidativo es un fenómeno que se desarrolla cuando la cantidad de especies reactivas de oxígeno (ROS) sobrepasa el balance entre la producción y capacitación generando consecuencias negativas en los procesos celulares 36, en los espermatozoides la producción de ROS se correlaciona negativamente con su calidad fisiológica, la formación de los ROS se ha relacionado con la infertilidad, un estudio realizado en hombres infértiles ha evidenciado la existencia de una mayor cantidad de ROS en estos pacientes en comparación con hombres fértiles 37, en adición a estos resultados otras investigaciones han determinado que los pacientes y donantes con parámetros normales en la movilidad espermática tienen una menor formación de ROS respecto a los que presentaban una movilidad espermática anormal 38, sin embargo niveles bajos de especies reactivas de oxígeno, son necesarias para el proceso de capacitación y fecundación 39.
Por lo tanto, el objetivo de este trabajo fue establecer los efectos que tiene la borra de café sobre la calidad seminal, determinando in vitro los cambios que esta puede generar sobre la movilidad y los parámetros funcionales de los espermatozoides humanos.
MATERIALES Y MÉTODOS
Muestras seminales
Se incluyeron 16 muestras de semen de voluntarios aparentemente sanos con una edad promedio de 24 años (20 a 28 años), sin hijos, con parámetros seminales normales y que no fumaran, la muestra seminal fue recolectada mediante masturbación después de un periodo de abstinencia sexual de 2 a 5 días y se evaluaron en un máximo de 2 horas después de su recolección 40. Cada individuo firmó un consentimiento informado aprobado por el Comité de Bioética, Facultad de Medicina, de la Universidad de Antioquia, después de leer y entender el propósito de la investigación.
A cada muestra de semen se le realizó la cuantificación de la movilidad por medio de microscopia a partir del lineamiento establecido por el manual de análisis seminal de la Organización Mundial de la Salud (OMS): movilidad tipo I (progresiva), movilidad tipo II (no progresiva), movilidad total (I+II) y movilidad tipo III (espermatozoides inmóviles).
Incubación directa de los espermatozoides y la dilución de la borra de café en PBS
En viales de 1.5 mL se realizó una dilución de los residuos del café seco (borra de café) con tampón fosfato salino (PBS, Gibco, Grand Island, NY, EE. UU.) a una concentración de 1.5 mg/mL. Se preparó una solución madre con el propósito de realizar todos los ensayos con similares condiciones y por lo tanto evitar alguna posible variación en la borra según la preparación o la temporada de preparación. Se preparó una dilución 1:2 de la muestra seminal con la borra de café y como control negativo la muestra de semen fue diluida 1:2 con PBS, se incubaron durante 2 horas a 37°C, cada 30 minutos se cuantifico al microscopio la movilidad espermática por duplicado.
Evaluación de las propiedades funcionales de los espermatozoides
Aproximadamente 1 x 106 espermatozoides fueron incubados con borra de café y PBS durante 60 minutos a una temperatura de 37 °C, con el propósito de determinar los parámetros funcionales espermáticos mediante citometría de flujo: potencial de membrana mitocondrial, producción de especies reactivas de oxígeno y lipoperoxidación de la membrana celular.
Evaluación de potencial de membrana mitocondrial (PMM)
Se evaluó usando la tinción con yoduro de 3,3’-di-hexiloxacarbocianina (DiOC6, Molecular Probes Inc., Países Bajos), un colorante lipofílico, catiónico y selectivo para mitocondrias de células vivas, este se caracteriza por mostrar el estado del potencial de la membrana mitocondrial. El yoduro de propidio (IP, Molecular Probes Inc., Países Bajos) se utilizó como tinción para discriminar los espermatozoides necróticos/muertos 37,41. Los datos fueron analizados como el porcentaje de espermatozoides vivos con alto y bajo PMM y de espermatozoides necróticos/muertos.
Evaluación de especies reactivad de oxígeno (ROS)
Se evaluaron midiendo los niveles intracelulares de ROS (H2O2, HO−ONNOO−) espermáticos, utilizando 2’,7’-diclorofluoresceína diacetato (DCFH-DA) con IP para excluir los espermatozoides necróticos/muertos. Los resultados se expresaron como el porcentaje de espermatozoides negativos para IP y positivos para DCFH-DA molécula de señal permeable no fluorescente, altamente sensible a cambios de oxidación/reducción 41.
Evaluación de lipoperoxidación de la membrana celular (LIPOPX)
Para evaluar el estado de lipoperoxidación de la membrana celular espermática se usó el colorante BODIPY (581/591) C11 (MolecularProbes Inc., Países Bajos) de acuerdo con el método propuesto por Aitken et al. 42. Los resultados se expresan como el porcentaje de espermatozoides que exhiben la respuesta de fluorescencia verde.
Análisis estadístico
Se realizó un análisis descriptivo determinando los valores de media y rango de la movilidad espermática evaluados cada 30 minutos durante las 2 horas de incubación a las que se expusieron los espermatozoides a la borra de café. Los resultados de citometría de flujo fueron analizados mediante el programa FlowJo (TreeStar, Inc. Oregon, USA). Adicionalmente, se realizó una prueba Wilcoxon para la comparación de los grupos, todas las determinaciones se realizaron mediante el programa estadístico GraphPad Prism 8.0 (GraphPad Software, San Diego, CA, EE. UU.) y se consideró un nivel mínimo de significancia del 95%, valor p de 0.05.
RESULTADOS
El análisis del efecto de la borra de café sobre los espermatozoides, fueron divididos según el tipo de movilidad I (progresiva), II (no progresiva), I+II (movilidad total) y III (inmóviles), se compararon en función del tiempo con respecto al control negativo.
Se observaron cambios significativos en la movilidad tipo I, I+II y III, en los cuales se presenta una disminución de la movilidad en muestras que fueron incubadas sin el estímulo desde los 30 minutos y un aumento de la movilidad en las muestras incubadas con la borra de café (Figura 1 A-B y Figura 2 A-B). El mayor efecto de la borra de café sobre la movilidad tipo I de los espermatozoides se observó entre los 60 (49,81 ± 16,51) y 90 minutos (48,63 ± 12,97) post incubación (Tabla 1), en contraste, la muestra control desde los 30 minutos (38,8 ± 14,98) evidencia un descenso en la movilidad espermática, esta tendencia se manifestó de forma significativa entre el control y la borra de café en los mismos tiempos para la movilidad total y para los espermatozoides inmóviles (Tabal 1).
La borra de café incremento el potencial de membrana mitocondrial (14.4%) respecto a la muestra sin estímulo (7.9%, p=0,03, Figura 3A), no obstante, no se encontró una diferencia significativa en los valores de intensidad media de fluorescencia entre estas poblaciones (Figura 3B).
Al evaluar la producción de ROS de las muestras seminales no se observaron diferencias significativas al comparar los valores obtenidos para las muestras con el estímulo en contraposición a aquellas que no lo tenían (p>0.05, Figura 3C).
Finalmente, el estado de la lipoperoxidación de la membrana espermática no evidencio alteración en las muestras con el estímulo y aunque la diferencia con respecto al grupo control es estadísticamente no significativo (p>0,05), las muestras con el estímulo si mostraron un menor porcentaje (Figura 3C) de espermatozoides con lipoperoxidación de la membrana y una menor intensidad media de fluorescencia (Figura 3D).
DISCUSIÓN
En el presente estudio, se realizó la evaluación in vitro del efecto de la borra de café sobre la biológía espermática, los hallazgos de este estudio evidencian que la borra de café (1.5 mg/mL) afecta positivamente la movilidad.
La borra de café contiene niveles de cafeína variables (arábica (0.5%) o robusta (0.2%) 10, existen estudios en los cuales se evidencia que la administración oral de 5 mg/kg o 300 mg de cafeína induce una concentración plasmática de 10 µg/mL 43,44, otros demuestran que el consumo diario de 240-300 mg de cafeína es equivalente a la ingesta de 3-7 mg de cafeína/kg de peso corporal en un adulto 45, Beach et al., evaluaron la capacidad que tiene la cafeína de excretarse en el semen, comparándolo con las concentraciones de cafeína en sangre, evidenciando que la cafeína puede equilibrar su concentración entre la sangre y los órganos accesorios de la reproducción logrando así ser secretada en el eyaculado, a su vez determinaron que una dosis de hasta 400 mg de cafeína no afectan la concentración, ni el volumen espermático 46, el consumo de café/te durante las últimas 24 horas antes de la eyaculación en 209 pacientes evidencio como resultado más significativo la disminución en la fragmentación de ADN espermático 47, además estudios in vitro en muestras seminales de jabalí congelados y descongelados por cafeína y adenosina, demostraron que la cafeína incrementa la incidencia de penetración al oocito, también se evidencio que la cafeína logro un efecto mucho mayor en la capacitación de los espermatozoides y permitió la reacción acrosómica espontanea 48.
La cafeína es un compuesto que se encuentra además del café, en él te, las bebidas carbonatadas, medicamentos no prescritos y otros alimentos (cacao, helado y tortas). La cafeína cruza con facilidad las membranas biológicas (gastrointestinal, hematoencefálica y placentaria) lo que le permite distribuirse rápidamente por todo el cuerpo 49, además cuenta con la capacidad de hidrolizar las grasas logrando producir ácidos grasos libres y de inhibir la lipoperoxidación que se da por medio de los radicales hidroxilo (OH), peróxidos (ROO) y moléculas de oxígeno en estado de excitación (oxigeno singlete) 49-52. El café también cuenta con componentes como el ácido clorogénico el cual se encuentra conformando entre 70-350 mg de una taza de café de 200 mL de los cuales son absorbidos en el intestino alrededor del 33% 53,54, este compuesto cuenta con gran capacidad antioxidante en todas las presentaciones de producción como el café verde, tostado y subproductos relacionados (pulpa, mucilago, pergamino y borra) 54.
La borra se obtiene a partir de la preparación del café soluble y representa la parte insoluble del grano de café tostado que en la actualidad se presenta como un problema de contaminación para la industria cafetera difícil de ser degradado y que necesita de mucho tiempo para ser eliminado parcialmente por la acción microbiana 55, por esta razón se han estudiado posibilidades en la utilización de la borra de café para la producción de biocombustibles, de proteínas y hongos comestibles, además de variables como medio para la elaboración de papel 55 y basados en los resultados de este estudio como un activador de espermatozoides humanos.
En cuanto a utilidades dirigidas al ámbito de la salud no existe evidencia científica que muestre la implementación de la borra de café, sin embargo, investigadores como Félix O et al., han demostrado al valorar la actividad antioxidante y el contenido de metabolitos antioxidantes en muestras de café pergamino tipo Arábica, que en el proceso de tostación de grado medio se da un aumentó en el contenido de metabolitos secundarios como fenoles y flavonoides, además de aumentar la actividad antioxidante 56, con esta misma idea Fonseca García L et al. al evaluar la capacidad antioxidante y el contenido de fenoles totales en café y subproductos del mismo, han obteniendo en muestras comerciales y muestras sin tostar registros positivos de fenoles totales y capacidad antioxidante 57, así mismo en un estudio publicado en 2013 en el cual se buscaba recuperar antioxidantes naturales de la borra de café, se determinó que todos los residuos recolectados mostraban grandes cantidades de fenoles totales y una alta capacidad antioxidante en extractos que usaron como disolvente el etanol 58, por el contrario, el incremento de la temperatura y el tiempo por encima del grado medio en el proceso de tostión genera un efecto negativo sobre la actividad antioxidante, esto se evidencio en la demostración de Bernard A. Goodman et al., el cual expone el café instantáneo a unas temperaturas de 27-77 °C otorgándole características prooxidantes que le permiten comportarse como fuente de radicales libres para la molécula de ácido ascórbico 59.
Los cambios significativos observados en el presente estudio sobre la movilidad espermática pueden obedecer a la existencia de concentraciones altas de antioxidantes en la borra de café, según el estudio realizado por B. Rodríguez-Alonso et al., sobre 78 muestras seminales evidencio que en todas aquellas que contenían un nivel elevado de estrés oxidativo se presentó un incremento en la fragmentación del ADN espermático con una progresión de 2.5% por cada hora transcurrida en comparación con las muestras que tenían una estabilidad en la fragmentación del ADN 60, el estrés oxidativo altera la capacidad fecundante 39, y los antioxidantes contrarrestan el efecto nocivo de los radicales 61.
El estrés oxidativo se genera cuando los niveles de ROS exceden la capacidad antioxidante, aunque las ROS tienen un papel primordial durante una seria de eventos espermáticos, su aumenta afecta la calidad seminal, causando infertilidad 36,62,63. El aumento del estrés oxidativo resulta en la alteración de las características espermáticas al inducir la peroxidación lipídica de la membrana plasmática de los espermatozoides, la oxidación de espermatozoides cruciales proteínas y fragmentación del ADN espermático, lo que lleva a la infertilidad masculina 64-66}.
Reciente dos trabajos publicados por dos de los grupos más prestigiosos en los antioxidantes y la fertilidad 67,68, confirman el papel importante que juegan los antioxidantes. El profesor Aitken 67 reafirma la importancia de controlar el estrés oxidativo en múltiples eventos, incluso algunos de estilo de vida modificables, lo cual permitir repercutir positivamente sobre la calidad seminal, mientras que el otro grupo demuestra que el tratamiento con antioxidantes durante tres meses mejora la calidad seminal, parámetros convencionales y funcionales, en hombres con infertilidad idiopática 68.
Finalmente, en los espermatozoides las mitocondrias son orgánulos de mucha importancia, tienen como función principal el producir ATP 69, daños en su estructura se relacionan con una disminución drástica de la movilidad espermática 70, algunos de estos daños se relacionan con la producción de ROS 71, en el presente estudio se observó que los espermatozoides que se encontraban con el estímulo de la borra de café presentaron un mayor PMM lo que sugiere que los extractos de borra de café generan una mayor actividad mitocondrial esto viéndose reflejado en el aumento de la movilidad espermática tipo I y I+.
CONCLUSIONES
La borra de café, seguramente debido a los compuestos antioxidantes, afecta positivamente la movilidad espermática aumentando el potencial de membrana mitocondrial. Por lo tanto, esto es un paso inicial en la búsqueda de un suplemento de origen natural que aumente la calidad seminal in vitro.
REFERENCIAS
- Organization IC. Coffee Market Report2019.
- Belitz H, Grosch W, Schieberle P. Food chemistry. 2009. Milk and Dairy Products:498-545.
- Gotteland M, de Pablo V S. Algunas verdades sobre el café. Revista chilena de nutrición 2007;34:105-15.
- Figueroa-Hernández E, PÉREZ-SOTO F, GODÍNEZ-MONTOYA L. La producción y el consumo del café. ECORFAN Madrid, España 2015.
- Higdon JV, Frei B. Coffee and health: a review of recent human research. Critical reviews in food science and nutrition 2006;46:101-23.
- Spiller MA. The chemical components of coffee. Caffeine 1998;1998:97-161.
- Rivera Serna JS. Estudio de la influencia del método de Tostión en la calidad sensorial del café: Universidad Nacional de Colombia-Sede Bogotá; 2017.
- RODRIGUEZ N, Zambrano D. Los subproductos del café: fuente de energía renovable2013. Report No.: 0120-0178.
- Gonzalez LVP, Gómez SPM, Abad PAG. Aprovechamiento de residuos agroindustriales en Colombia. RIAA 2017;8:141-50.
- Campos-Vega R, Loarca-Pina G, Vergara-Castañeda HA, Oomah BD. Spent coffee grounds: A review on current research and future prospects. Trends in Food Science & Technology 2015;45:24-36.
- Lozano RP, García YA, Tafalla DB, Albaladejo MF. Cafeína: un nutriente, un fármaco, o una droga de abuso. Adicciones 2007;19:225-38.
- Nawrot P, Jordan S, Eastwood J, Rotstein J, Hugenholtz A, Feeley M. Effects of caffeine on human health. Food Additives & Contaminants 2003;20:1-30.
- Duro Mota E, Causín Serrano S, Campillos Páez MT, Vallés Ugarte M. Consumo de cafeína y riesgo de aborto espontáneo en el primer trimestre. Medifam 2001;11:105-8.
- Nordestgaard AT, Thomsen M, Nordestgaard BG. Coffee intake and risk of obesity, metabolic syndrome and type 2 diabetes: a Mendelian randomization study. International journal of epidemiology 2015;44:551-65.
- Santos RMM, Lima DRA. Coffee consumption, obesity and type 2 diabetes: A mini-review. European journal of nutrition 2016;55:1345-58.
- Gaeini Z, Bahadoran Z, Mirmiran P, Azizi F. Tea, coffee, caffeine intake and the risk of cardio-metabolic outcomes: findings from a population with low coffee and high tea consumption. Nutrition & metabolism 2019;16:28.
- O’Keefe JH, Bhatti SK, Patil HR, DiNicolantonio JJ, Lucan SC, Lavie CJ. Effects of habitual coffee consumption on cardiometabolic disease, cardiovascular health, and all-cause mortality. Journal of the American College of Cardiology 2013;62:1043-51.
- Yu MC, Mack TM, Hanisch R, Cicioni C, Henderson BE. Cigarette smoking, obesity, diuretic use, and coffee consumption as risk factors for renal cell carcinoma. Journal of the National Cancer Institute 1986;77:351-6.
- Salari-Moghaddam A, Milajerdi A, Surkan PJ, Larijani B, Esmaillzadeh A. Caffeine, Type of Coffee, and Risk of Ovarian Cancer: A Dose–Response Meta-Analysis of Prospective Studies. The Journal of Clinical Endocrinology & Metabolism 2019;104:5349-59.
- Hernán MA, Takkouche B, Caamaño‐Isorna F, Gestal‐Otero JJ. A meta‐analysis of coffee drinking, cigarette smoking, and the risk of Parkinson’s disease. Annals of neurology 2002;52:276-84.
- Acheson KJ, Zahorska-Markiewicz B, Pittet P, Anantharaman K, Jéquier E. Caffeine and coffee: their influence on metabolic rate and substrate utilization in normal weight and obese individuals. The American journal of clinical nutrition 1980;33:989-97.
- Gorji Z, Nazary-Vannani A, Varkaneh HK, et al. The effect of green-coffee extract supplementation on obesity: A systematic review and dose-response meta-analysis of randomized controlled trials. Phytomedicine 2019:153018.
- Voskoboinik A, Kalman JM, Kistler PM. Caffeine and arrhythmias: time to grind the data. JACC: Clinical Electrophysiology 2018;4:425-32.
- Martínez-López S, Sarriá B, Mateos R, Bravo-Clemente L. Moderate consumption of a soluble green/roasted coffee rich in caffeoylquinic acids reduces cardiovascular risk markers: Results from a randomized, cross-over, controlled trial in healthy and hypercholesterolemic subjects. European journal of nutrition 2019;58:865-78.
- Turnbull D, Rodricks JV, Mariano GF, Chowdhury F. Caffeine and cardiovascular health. Regulatory Toxicology and Pharmacology 2017;89:165-85.
- Agardh E, Carlsson S, Ahlbom A, et al. Coffee consumption, type 2 diabetes and impaired glucose tolerance in Swedish men and women. Journal of internal medicine 2004;255:645-52.
- Whayne TF. Una taza de café y otras terapias alternativas en medicina clínica. Revista costarricense de cardiología 2009;11:41-6.
- Arab L. Epidemiologic evidence on coffee and cancer. Nutrition and cancer 2010;62:271-83.
- Nieto JGR, San Pedro EM, Luciano AG, Coronado JLB. Efectos del consumo de café para la salud cardiovascular, la diabetes y el desarrollo de cáncer. Psicothema 2004;16:531-47.
- Armstrong BG, McDonald AD, Sloan M. Cigarette, alcohol, and coffee consumption and spontaneous abortion. American journal of public health 1992;82:85-7.
- Leelarungrayub D, Sallepan M, Charoenwattana S. Effects of acute caffeinated coffee consumption on energy utilization related to glucose and lipid oxidation from short submaximal Treadmill exercise in sedentary Men. Nutrition and metabolic insights 2011;4:NMI. S8299.
- Lyngsø J, Kesmodel US, Bay B, Ingerslev HJ, Andersen A-MN, Ramlau-Hansen CH. Impact of female daily coffee consumption on successful fertility treatment: a Danish cohort study. Fertility and sterility 2019.
- Karmon AE, Toth T, Chiu YH, et al. Male caffeine and alcohol intake in relation to semen parameters and in vitro fertilization outcomes among fertility patients. Andrology 2017;5:354-61.
- Jensen TK, Swan SH, Skakkebæk NE, Rasmussen S, Jørgensen N. Caffeine intake and semen quality in a population of 2,554 young Danish men. American journal of epidemiology 2010;171:883-91.
- Goldstein A, Warren R. Passage of caffeine into human gonadal and fetal tissue. Biochemical pharmacology 1962;11:166-8.
- Mayorga Torres B, Camargo M, Cadavid ÁP, Maya C, Walter D. Estrés oxidativo: ¿un estado celular defectuoso para la función espermática? Revista chilena de obstetricia y ginecología 2015;80:486-92.
- Mayorga-Torres B, Cardona-Maya W, Cadavid A, Camargo M. Evaluación de los parámetros funcionales espermáticos en individuos infértiles normozooespérmicos. Actas urológicas españolas 2013;37:221-7.
- Agarwal A, Ikemoto I, Loughlin KR. Relationship of sperm parameters with levels of reactive oxygen species in semen specimens. The Journal of urology 1994;152:107-10.
- Iraizoz Barrios AM. Influencia del estrés oxidativo seminal en el resultado de técnicas de fertilización in vitro. 2017.
- Organization WH. WHO laboratory manual for the examination and processing of human semen. 2010.
- Acevedo PCL, Maya WDC. Selección espermática in vitro: espermatozoides con mejores características funcionales. Urología Colombiana 2017;26:26-33.
- Aitken RJ, Wingate JK, De Iuliis GN, McLaughlin EA. Analysis of lipid peroxidation in human spermatozoa using BODIPY C11. MHR: Basic science of reproductive medicine 2007;13:203-11.
- Blanchard J, Sawers S. The absolute bioavailability of caffeine in man. European journal of clinical pharmacology 1983;24:93-8.
- Alvi SN, Hammami MM. Validated HPLC method for determination of caffeine level in human plasma using synthetic plasma: application to bioavailability studies. Journal of chromatographic science 2011;49:292-6.
- Mandel H. Update on caffeine consumption, disposition and action. Food and Chemical Toxicology 2002;40:1231-4.
- BEACH CA, BIANCHINE JR, GERBER N. The excretion of caffeine in the semen of men: pharmacokinetics and comparison of the concentrations in blood and semen. The Journal of Clinical Pharmacology 1984;24:120-6.
- Varea RL. Efecto de los factores ambientales en la calidad espermática del hombre: Universitat Autònoma de Barcelona; 2017.
- Funahashi H, Nagai T. Regulation of in vitro penetration of frozen–thawed boar spermatozoa by caffeine and adenosine. Molecular Reproduction and Development: Incorporating Gamete Research 2001;58:424-31.
- Dlugosz L, Bracken MB. Reproductive effects of caffeine: a review and theoretical analysis. Epidemiologic reviews 1992;14:83-100.
- Shi X, Dalal N, Jain A. Antioxidant behaviour of caffeine: efficient scavenging of hydroxyl radicals. Food and chemical toxicology 1991;29:1-6.
- Devasagayam T, Kamat J, Mohan H, Kesavan P. Caffeine as an antioxidant: inhibition of lipid peroxidation induced by reactive oxygen species. Biochimica et Biophysica Acta (BBA)-Biomembranes 1996;1282:63-70.
- León-Carmona JR, Galano A. Is caffeine a good scavenger of oxygenated free radicals? The Journal of Physical Chemistry B 2011;115:4538-46.
- Chaves C, Esquivel P. Ácidos clorogénicos presentes en el café: capacidad antimicrobiana y antioxidante. Agronomía Mesoamericana 2019;30:299-311.
- Esquivel P, Jiménez VM. Functional properties of coffee and coffee by-products. Food Research International 2012;46:488-95.
- Paz JEW, Guyot S, Herrera RR, et al. Alternativas Actuales para el Manejo Sustentable de los Residuos de la Industria del Café e del Café en México Current Alternatives for Sustainable Management of Coffee Industry By Current Alternatives for Sustainable Management of Coffee Industry By-Products Products in Mexico. Revista Científica de la Universidad Autónoma de Coahuila 2013;5.
- Díaz FO, Ormaza AM, Rojano BA. Efecto de la Tostión del Café (Coffea arabica L. var. Castillo) sobre el Perfil de Taza, Contenido de Compuestos Antioxidantes y la Actividad Antioxidante. Información tecnológica 2018;29:31-42.
- FONSECA-GARCÍA L, CALDERÓN-JAIMES LS, Rivera ME. Capacidad antioxidante y contenido de fenoles totales en café y subproductos del café producido y comercializado en Norte de Santander (Colombia). Vitae 2014;21:228-36.
- Panusa A, Zuorro A, Lavecchia R, Marrosu G, Petrucci R. Recovery of natural antioxidants from spent coffee grounds. Journal of agricultural and food chemistry 2013;61:4162-8.
- Goodman BA, Glidewell SM, Deighton N, Morrice AE. Free radical reactions involving coffee. Food chemistry 1994;51:399-403.
- Rodríguez-Alonso B, López-Fernández C, Núñez-Calonge R, et al. Impacto del estrés oxidativo en la dinámica de fragmentación del ADN espermático. Medicina Reproductiva y Embriología Clínica 2016;3:137-43.
- Sánchez-Valle V, Méndez-Sánchez N. Estrés oxidativo, antioxidantes y enfermedad. Médica Sur 2018;20:161-8.
- Mayorga-Torres JM, Agarwal A, Roychoudhury S, Cadavid A, Cardona-Maya WD. Can a Short Term of Repeated Ejaculations Affect Seminal Parameters? J Reprod Infertil 2016;17:177-83.
- Mayorga-Torres BJM, Camargo M, Cadavid AP, du Plessis SS, Cardona Maya WD. Are oxidative stress markers associated with unexplained male infertility? Andrologia 2017;49.
- Aitken RJ, Koppers AJ. Apoptosis and DNA damage in human spermatozoa. Asian journal of andrology 2011;13:36.
- Agarwal A, Virk G, Ong C, Du Plessis SS. Effect of oxidative stress on male reproduction. The world journal of men’s health 2014;32:1-17.
- Mayorga Torres JM, Peña B, Cadavid AP, Cardona Maya WD. La importancia clínica del ADN espermático en el análisis seminal cotidiano. Revista chilena de obstetricia y ginecología 2015;80:265-8.
- Aitken RJ. Impact of oxidative stress on male and female germ cells: implications for fertility. Reproduction 2020;159:R189-R201.
- Arafa M, Agarwal A, Majzoub A, et al. Efficacy of Antioxidant Supplementation on Conventional and Advanced Sperm Function Tests in Patients with Idiopathic Male Infertility. Antioxidants (Basel) 2020;9.
- Allauca P, Ugarelli A, Santiani A. Determinación del potencial de membrana mitocondrial mediante citometría de flujo durante el proceso de criopreservación de espermatozoides epididimarios de alpacas. Revista de Investigaciones Veterinarias del Perú 2019;30:288-98.
- Amaral A, Lourenço B, Marques M, Ramalho-Santos J. Mitochondria functionality and sperm quality. Reproduction 2013;146:R163-R74.
- Paparella CV, Pavesi AB, Feldman RN, Bouvet BR. Importancia de la evaluación del estrés oxidativo en el semen humano. 2
TABLAS Y FIGURAS
Tabla 1. Valores consolidados para la movilidad espermática. Evaluación en porcentaje de la movilidad tipo I, I+II y III de los espermatozoides incubados con la borra de café (1.5 mg/mL) en función del tiempo.
| Movilidad I | ||||||||
| 30 minutos | 60 minutos | 90 minutos | 120 minutos | |||||
| Borra | Control | Borra | Control | Borra | Control | Borra | Control | |
| Media | 49,53 | 38,8 | 49,81 | 38,69 | 48,63 | 37,06 | 47,73 | 37,47 |
| DS | 15,04 | 14,98 | 16,51 | 15,97 | 12,97 | 14,8 | 12,83 | 14,5 |
| Movilidad I+II | ||||||||
| Media | 60,67 | 55,13 | 59,69 | 52,38 | 59 | 50,5 | 54,8 | 49,93 |
| DS | 10,85 | 10,28 | 12,68 | 13,68 | 9,338 | 13,4 | 11,39 | 11,49 |
| Movilidad III | ||||||||
| Media | 38,87 | 44,4 | 39,38 | 47,19 | 40,25 | 48,94 | 43,67 | 49,53 |
| DS | 10,97 | 10,38 | 12,79 | 13,64 | 9,518 | 13,55 | 11,13 | 11,53 |

Figura 1. Movilidad espermática tipo I. A. Evaluación del efecto de la borra de café (1.5 mg/mL) en proporción 1:2 sobre la movilidad espermática tipo I en función del tiempo (30, 60, 90 y 120 minutos). B. Consolidado de los resultados.
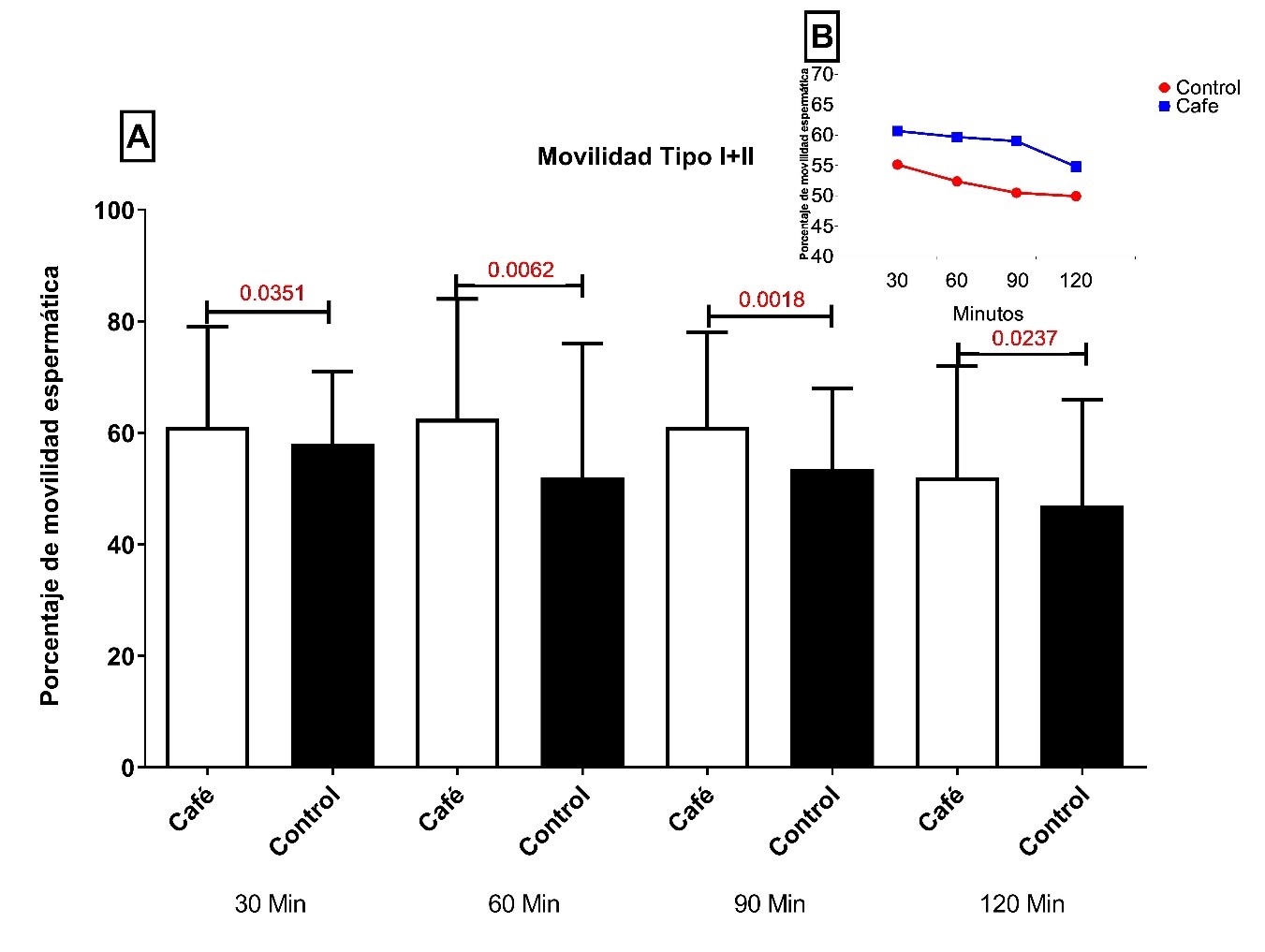
Figura 2. Movilidad esperm
histograma reproressentatico () vos para la lipoperoxidaciática total. A. Resultados del efecto de la borra de café (1.5 mg/mL) en proporción 1:2 sobre la movilidad espermática total en función del tiempo (30, 60, 90 y 120 minutos). B. Consolidado de los resultados.
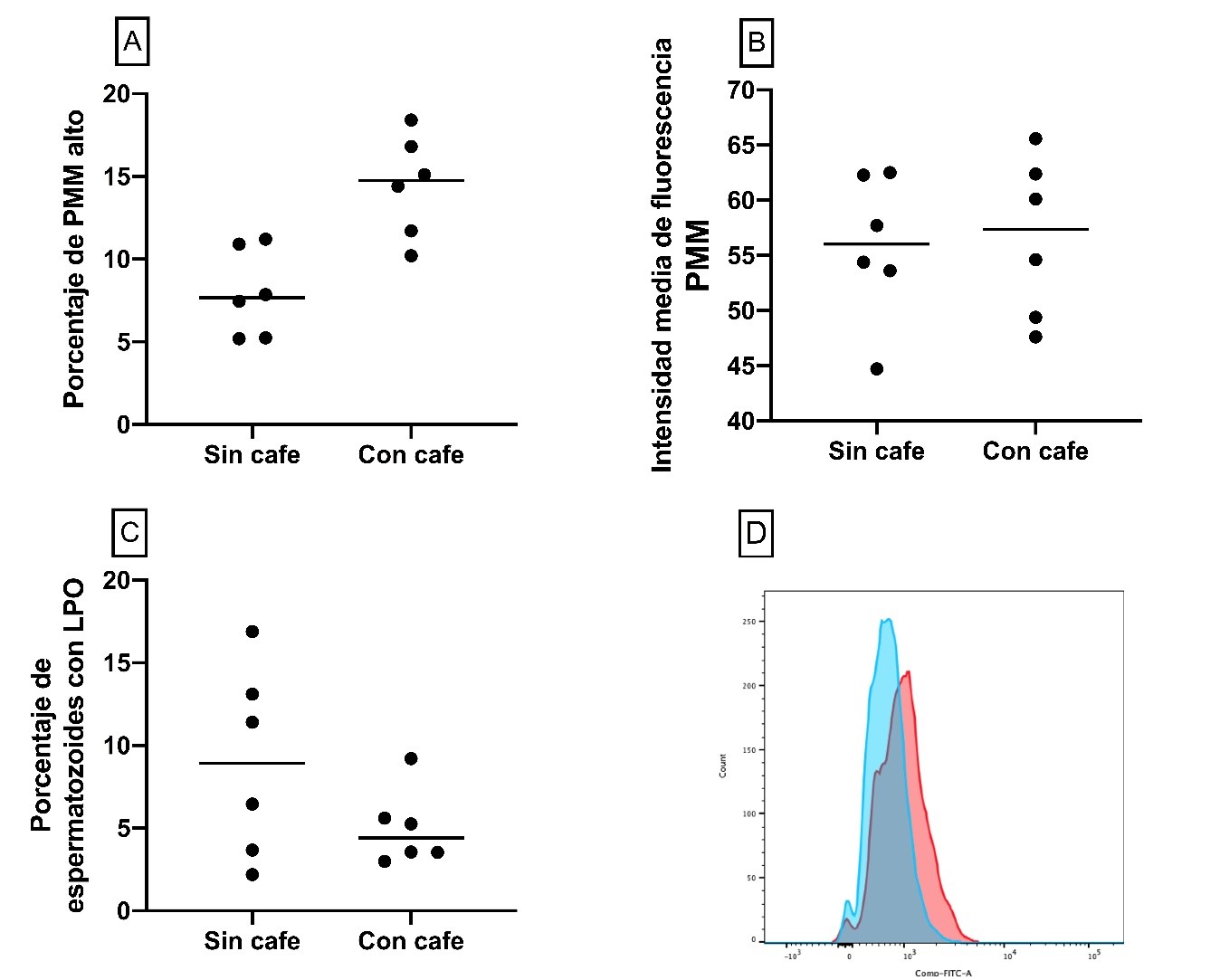
Figura 3. Pruebas espermáticas funcionales. Evaluación del porcentaje de celulas con potencial de membrana mitocondrial alto (PMM, A, p=0,03) e intensidad media de fluorescencia (B, p>0,05). Distribución (C) e histograma representativo (D) del porcentaje de espermatoozides positivos para la lipoperoxidación de la membrana espermática (p>0,05).



