2007
2
Autores:
Antonio Carvajal M.1, Italo Braghetto M.2, Rodrigo Carvajal G.3, Cristián Miranda V.1
Instituciones:
1Departamento de Obstetricia y Ginecología, Hospital Clínico Universidad de Chile, 2Departamento de Cirugía, Hospital Clínico Universidad de Chile, 3Becado de Gineco-Obstetricia, Hospital Clínico, Universidad de Chile.
Tipo de documento:
Trabajos OriginalesEndometriosis de la pared abdominal
Contenido del documento:
INTRODUCCIÓN
La endometriosis es definida como la presencia de estroma y glándulas endometriales fuera de la cavidad uterina (1-4). La endometriosis puede ser intra o extrapélvica. Nos referimos a endometrioma a una masa bien circunscrita de tejido endometrial localizado fuera de la pelvis (2,3). Los endometriomas de la pared abdominal (EPA) usualmente son procesos secundarios a cicatrices quirúrgicas ginecoobstétricas, como es la cicatriz de la cesárea (4).
Cuando se plantea el diagnóstico clínico, frecuentemente se confunde con otras masas que se localizan en la pared abdominal: lipomas, granulomas de suturas, hernias incisionales, quistes sebáceos, hematomas, sarcomas o metástasis (3,5).
En el presente estudio hacemos una revisión de la historia clínica de catorce pacientes con EPA, haciendo especial énfasis en la presentación clínica, diagnóstico diferencial, tratamiento y evolución.
PACIENTES Y MÉTODOS
Se analizaron las fichas clínicas de todas las pacientes hospitalizadas entre 01 de enero de 1997 al 31 de diciembre de 2005 en el Hospital Clínico de la Universidad de Chile, por masas de la pared abdominal, cuyo diagnóstico histológico correspondió a endometriosis. Se registró la presentación clínica, el diagnóstico presuntivo, los exámenes de laboratorio e imágenes (ecografía, TAC, RNM), los tratamientos y la evolución. Las variables continuas se presentan en promedios, rangos y frecuencia relativa.
RESULTADOS
De todas las pacientes con el diagnóstico de masa de la pared abdominal, sólo 14 correspondía a EPA. La edad promedio de presentación fue de 33,2 años (rango: 21-48 años). Todas las pacientes habían tenido, o una cirugía ginecológica (14,2%) u obstétrica (85,7%). Dos cistectomías laparoscópicas y 12 cesáreas respectivamente.
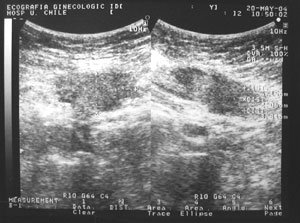
Los síntomas identificados fueron masa de la pared abdominal en todas las pacientes (n=14), dolor cíclico (71,4%), dolor no cíclico (28,5%), dispareunia (21,4%) y dismenorrea 42,8% (Tabla I). Las masas de la pared abdominal tenían como diámetro promedio 3,2 cm (rango: 2-7cm) medidos mediante ecografía transabdominal (Figura 1), y localizadas alrededor de las cicatrices abdominales en el 100% de los casos. El período entre la cirugía previa y el inicio de las manifestaciones clínicas varió entre dos meses y catorce años, con un promedio de 3,5 años (Tabla I). El diagnóstico preoperatorio fue correcto en 11 pacientes (64,3%). Basado principalmente en la presencia de masa dolorosa abdominal localizada en una cicatriz de laparotomía que empeoraba con las menstruaciones. Al otro 35,7% (n=5) de las pacientes se les diagnosticó granulomas (3 pacientes), lipoma (1 paciente) y hernia inguinal (1 paciente) (Tabla I).
Se realizó estudio ultrasonográfico en todas las pacientes. Mostrando masas quísticas de contornos regulares (Figura 1). Tres pacientes tenían TAC que revelaba compromiso de los rectos abdominales, en estas pacientes se planificó una cirugía con escisión amplia y refuerzo con mallas de polytetrafluoethyleno.
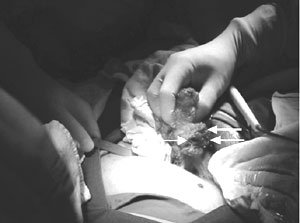
El diagnóstico definitivo se confirmó mediante histopatología de las piezas operatorias, donde se encontró estroma y glándulas ectópicas de endometrio. Todas las pacientes con diagnóstico correcto pre operatorio de EPA (64,3%), se les realizó exploración quirúrgica con escisión amplia de los endometriomas, dejando límites libres de al menos 1 cm (Figura 2). En las pacientes con diagnóstico inicial incorrecto (35,7%) sólo se les realizó resección amplia, sin verificar límites libres de enfermedad. Las pacientes con compromiso profundo de la enfermedad hasta aponeurosis, fue necesario usar mallas de polytetrafluoethyleno para corregir los defectos (64,3%) (Tabla I).
Cuatro pacientes (28,5%) presentaron recurrencias de la EPA. Tres (75%) fueron aquellas con diagnóstico pre operatorio incorrecto. De las pacientes con diagnóstico pre operatorio incorrecto, 60% presentó recurrencias comparado con el 11,1% de recurrencias en el grupo con diagnóstico inicial correcto, donde se realizaron cirugías con escisión amplia y límites libres de endometriosis.
DISCUSIÓN
La endometriosis es diagnosticada en el 30% de los casos referidos por infertilidad y en el 10-70% de las mujeres con dolor pélvico (6). Estudios estiman que puede afectar alrededor 7-15% de todas las mujeres en edad reproductiva, haciendo de ésta una condición frecuente. Es curioso que sólo a una paciente de nuestra serie se le diagnosticara previamente endometriosis.
Reportes indican que la endometriosis puede estar presente entre 0,03% y 0,47% de las cicatrices de cesárea (5,7,8), pero que también puede encontrarse alejada de ellas como episiotomías, hernioplastias e histerectomías vaginales (9). Si la EPA se desarrolló cuando fue necesaria una histerectomía obstétrica, depende de las semanas de gestación. Por ejemplo, si se realiza en el segundo trimestre de gestación la incidencia es 1,08% pero en las semanas finales del embarazo es 0,03%. La decidua temprana tiene capacidad pluripotencial y puede producir replicación celular dando origen a un endometrioma (7,10). En esta revisión encontramos dos pacientes con procedimientos laparoscópicos previos como cirugía causal de los implantes extra peritoneales, tal como se ha reportado en la literatura, en los sitios de inserción de los trocares. También hay reportes posteriores a amniocentesis y hernioplastias (11,12). El desarrollo de un endometrioma en una cicatriz de laparotomía es probablemente mejor explicada por diseminación de implantes endometriósicos preexistentes en la cavidad abdominal hacia la herida operatoria (2). Aunque la contaminación residual de la herida operatoria con decidua después de una cesárea es inevitable, el desarrollo de EPA es muy raro. Esto sugiere una predisposición hereditaria y la existencia de características biológicas en el endometrio de estas pacientes que facilitan el desarrollo de esta patología, por lo que podría ser importante hacer esfuerzos para disminuir la contaminación residual de las laparotomías y prevenir la implantación de endometrio ectópico (4). Sin embargo, la implantación directa no podría explicar las EPA que ocurren sin cirugías previas. Se ha descrito EPA espontáneas (8,13), que podría corresponder a transplantes linfáticos o metaplasia.
Como en otros estudios, los pacientes presentaron síntomas meses a años después de su intervención quirúrgica (8,14,15). Presentando síntomas tempranamente a menores edades, probablemente a la mejor vitalidad de los implantes endometriales o a la exposición a elevados niveles de estrógenos que inducen proliferación.
Es raro el desarrollo de endometriosis en la menopausia, pero es posible que se manifieste posterior al uso de terapia de reemplazo hormonal que activa antiguos implantes endometriósicos.
El diagnóstico diferencial debe ser hecho con hernias, lipomas, abscesos, teratomas, sarcomas y cáncer metastásico (3,5,7,8). Usualmente presentan la clásica tríada de masa, dolor cíclico y cicatriz de laparotomía previa, pero no siempre. Las masas generalmente son sólidas, densas y bien circunscritas. El dolor se puede correlacionar o no con el ciclo menstrual. En nuestra casuística la clínica permitió un correcto diagnóstico en el 64,3%.
En endometriomas muy superficiales, puede ocurrir ulceración en enfermedad prolongada, pero es muy raro (2). El diagnóstico en las pacientes con cicatriz de cesárea no es difícil de lograr, basta con tener la patología en mente para poder sospecharla (4,8,9). En las pacientes que presentan un cuadro típico, es necesario recurrir a procedimientos adicionales para descartar los diagnósticos diferenciales, determinar el tamaño de las lesiones y excluir patología intraabdominal concomitante (7, 8,9). En nuestra revisión se utilizó la ecografía transabdominal con muy buenos resultados, siendo innecesario en la mayoría de los casos el TAC o la RNM.
Se ha reportado el uso de biopsia de aspiración con aguja fina para confirmar el diagnóstico y excluir malignidad (16,17), pero otros trabajos publicados han mostrado utilidad escasa e incluso aumento de la recurrencia (8,18). Por lo tanto, el citodiagnóstico de endometriosis en general no es recomendable, sobretodo si el cuadro clínico es claro y más aún si posee altos falso negativos en lesiones pequeñas (8,18).
El estudio de imágenes no aporta resultados específicos, pero ayuda a determinar la extensión de la enfermedad y el compromiso de la pared abdominal para planificar la cirugía posterior (8,9, 15). La apariencia ecográfica de los EPA puede ser de características quística, mixta o sólida (19). Estos patrones no se correlacionan con el ciclo menstrual y son inespecíficos. Por otro lado, si se realiza al inicio de la menstruación, el tamaño de las lesiones es mayor, y las lesiones pueden ser evidenciadas más fácilmente. Como ya hemos discutido, el TAC y la RNM son inespecíficos (20) y no aportan nada más que un examen ecográfico de buena calidad (19,20).
El manejo de la EPA puede ser médico o quirúrgico (6,8,9,15). El tratamiento médico se refiere al uso de anticonceptivos orales, progestinas y análogos de GnRH. Sólo se ha reportado el alivio transitorio de los síntomas y la recurrrencia es de regla al suspender la terapia (22). El manejo óptimo es mediante la escisión quirúrgica amplia con especial cuidado de remover todo el tejido afectado y dejando límites libres de enfermedad. El manejo médico debe considerarse solamente para reducir el dolor, o en el caso de análogos de GnRH para disminuir el tamaño de las lesiones previo a la cirugía.
La recurrencia es rara, usualmente se presenta dentro de un año y es producto de remoción inadecuada de tejido endometriósico (3,8,9,15). El éxito de la cirugía radica en respetar márgenes adecuados libres de enfermedad (3,15,21). En las pacientes en que las lesiones se extienden a través de la pared abdominal comprometiendo rectos abdominales o aponeurosis, es necesario resecar importante cantidad de tejido y debe usarse una malla de polytetrafluoethyleno como material de reparación (3,7,8,15,18,21).
La incidencia de endometriosis pélvica concomitante con EPA se ha reportado entre 14,3 y 26% (3,8,16,21), y puede ser aun mayor ya que no todas las pacientes son sometidas a exploración pélvica.
Se debe estar alerta ante la posibilidad de un carcinoma originado de un EPA. La incidencia se ha reportado entre 0,3 y 1% (23, 24, 25). La transformación maligna es un evento raro, descrito principalmente complicando endometriosis ovárica, pero debe ser reconocida como una posibilidad en el diagnóstico diferencial de masas de la pared abdominal.
CONCLUSIONES
Siempre debemos pensar en la presencia de EPA cuando se observe una masa dolorosa y/o aumento de volumen y/o cambio de coloración de la piel en relación a una cicatriz de laparotomía (cesárea, histerectomías y procedimientos laparoscópicos). La ecografía es la técnica de imágenes de mayor utilidad. El tratamiento de elección es la extirpación con amplios márgenes para reducir las recurrencias. En los defectos de la pared abdominal se deben aplicar mallas de material sintético para evitar el desarrollo posterior de hernias de la pared abdominal. El tratamiento médico puede usarse como terapia complementaria para manejar el dolor previo a la cirugía. A pesar que la probabilidad de malignización es baja, siempre debe realizarse el estudio histológico.
BIBLIOGRAFÍA
- Strorment J, Brumsted J. Endometriosis. In: Curtis MG, Hopkins MP (eds): Glass’s Office Gynecology, Ed 5. Baltimore, Williams & Wilkins, 1998: 335-54.
- Koger KE, Shantney Ch, Hodge K, McClenathan JH. Surgical scar endometrioma. Surg Gynecol Obstet 1993;77:243-6.
- Blanco RG, Parithivel VS, Shah AK, et al. Abdominal wall endometriomas. Am J Surg 2003;185:596-8.
- Wasfie T, Gomez E, Seon S, Zado B. Abdominal wall endometrioma after cesarean section: a preventable complication. Int Surg 2002;87:175-7. 5. Yoram W, Haddad R, Werbin N, et al. Endometriosis in abdominal scar: diagnostic pitfall. Am J Surg 1996; 6:1042-4.
- Lapp T. ACOG Issues Recommendations for the Management of Endometriosis. American College of Obstetricians and Gynecologists. American Family Physicians 2000;62:1431-4.
- Singh K., Lessells A., Adam D., et al., Presentation of Endometrosis to general surgeons: a 10 years experience. Br J Surg 1995; 82: 1349-1351.
- Zhao X, Lang J, Leng J, Liu Z, Sun D, Zhu L. Abdominal wall endometriomas. Int J Gynaecol Obstet 2005; 90:218-22.
- Gunes M, Kayikcioglu F, Ozturkoglu, Haberal A. Incisional endometrosis after cesarean section, episiotomy and other gynecologic procedures. J Obstet Gynaecol Res 2005;31:471-5.
- Scott R, Telinde R. Clinical external endometriosis. Probable viability of menstrually shed fragmentts of endometrium. Obstet Gynecol 1999;42:699-711.
- Hughes M, Bartholomew D, Paluzzi M. Abdominal wall endometriosis after amniocentesis: a case report. J Reprod Med 1997;42:597-9.
- Healy J, Wilkinson N, Sawyer M. Abdominal wall endometrioma in a laparoscopic trocar tract: a case report. Am Surgeon 1995;61:962-3.
- Ideyi S, Schein M, Niazi M, Gerst P. Spontaneous endometriosis of the abdominal wall. Dig Surg 2003; 20:246-8.
- Dwivedi A, Agrawal S, Silva Y. Abdominal wall endometriomas. Dig Dis Sci 2002;47:456-61.
- Erkan N, Haciyanh M, Sayhan H. Abdominal wall endometriomas. Int J Gynaecol Obstet 2005;89:59-60.
- Wolf G, Singh K. Cesarean scar endometriosis: a review. Obstet Gynecol Surv 1989;44: 89-95.
- Fulciniti F, Caleo A, Lepore M, Fortunato A, Vetrani A, Palombini L. Fine needle cytology of endometriosis: experience with 10 cases. Acta Cytol 2005;49(5):495-9.
- Matthes G, Zabel D, Nastala C, Shestak K, Endometrioma of the abdominal wall following combined abdominoplasty and hysterectomy: case report and review of literature. Ann Plast Surg 1998;40:672-5.
- Francica G, Giardielo C, Angelone G, Finelli R, Tramonmnmtano G. Abdominal wall endometrioma near cesarean delivery scars. J Ultrasound Med 2003; 22:1041-7.
- Balleyguier C, Chapron C, Helenon O, Menu Y. Abdominal wall and surgical scar endometriosis: results of magnetic resonance imaging. Gynecol Obstet Invest 2003;55:220-4.
- Picod G, Boulanger L, Bounoua F, Leduc F, Duval G. Abdominal wall endometriosis after caesarean section: report of fifteen cases. Gynecol Obstet Fertil 2006; 34(1):8-13.
- Purvis R, Tyring S. Cutaneous and subcutaneous endometriosis: surgical and hormonal therapy. J Dermatol Surg Oncol 1994; 693-5.
- Park S, Hong S, Wu H, Ha S. Clear cell carcinoma arising in a cesarean section endometriosis: a case report. J Korean Med Sci 1999;14:217-9.
- Matter M, Schneider N, McKee T. Cystadenocarcinoma of the abdominal wall following caesarean section: case report and review of the literature. Gynecol Oncol 2003;91:438-43.
- Leng J, Lang J, Guo L, Li H, Liu Z. Carcinosarcoma arising from atypical endometriosis in a cesarean section scar. Int J Gynecol Cancer 2006;16(1): 432-5.