2020
4
Autores:
Fernando Manzur-Jattina,b, Hugo Corrales-Santanderc, Cristhyan Pacheco-Ayosb,d, Luis Fernando Carbonell-Riquettb,e ,Juan González-Oñateb,d, Andrea Ardila-Saenzb,f Angélica Manotas-Molinab,d, Libia Manotas-Molinab,e, Luznevis Pérez-Llerenab,f.
Instituciones:
a Cardiólogo, Master en ensayos clínicos, PhD Cardiología Anatomoclínica – Universidad Complutense de Madrid, Madrid, España.
b Centro de Investigaciones Biomédicas (CIB), Facultad de Medicina – Universidad de Cartagena, Cartagena de Indias, Colombia.
c Médico toxicólogo. Profesor Departamento de Medicina, Universidad del Norte, Barranquilla, Colombia.
d Médico, Facultad de Medicina – Universidad de Cartagena, Cartagena de Indias, Colombia.
e Médico, Facultad de Medicina – Universidad Libre, Barranquilla, Colombia.
f Médico, Facultad de Medicina – Universidad Del Sinu, Cartagena, Colombia.
Correspondencia: Luis Fernando Carbonell Riquett, luiscarbonell16@gmail.com
Tipo de documento:
Artículo de RevisiónEnfermedades cardio-metabólicas en el embarazo: Revisión sobre diagnóstico, tratamiento y proyección del riesgo cardiovascular a largo plazo
Contenido del documento:
INTRODUCCIÓN
Las enfermedades cardiovasculares siguen siendo la principal causa de muerte a nivel mundial; en 2015 se produjeron aproximadamente 17.7 millones de muertes en el mundo secundarias a estas.1
Se ha recopilado evidencia sobre la asociación entre patologías obstétricas y el riesgo cardiovascular a futuro2, despertando el interés por estudiar la gestación, y comorbilidades asociadas a dicha condición y su impacto en la salud cardiovascular.3
El embarazo se puede considerar como la principal prueba a la que puede ser sometido el cuerpo de la mujer. Este proceso lleva consigo cambios estructurales, funcionales, metabólicos y cardiovasculares; dichos cambios pueden generar una predisposición para el desarrollo de eventos adversos durante la misma gestación y en el periodo postparto.4
La presentación de patologías como trastornos hipertensivos del embarazo, diabetes gestacional, parto pretérmino y bajo peso al nacer, se han asociado a patologías de alto riesgo cardiovascular en el posparto, tanto a corto como mediano plazo.5,6
Fisiología cardiovascular en el embarazo
Durante el embarazo ocurren cambios fisiológicos necesarios en la mujer. Estos buscan favorecer que la gestación transcurra sin afecciones al feto en crecimiento.7 Lo anterior, se traduce en adaptaciones hemodinámicas que son de vital importancia en los desenlaces materno -fetales.8
La disminución de la RVP secundaria a la vasodilatación producida por el aumento del óxido nítrico (ON) y los efectos de la progesterona a nivel muscular; activan mecanismos de compensación a nivel del eje renina – angiotensina – aldosterona para garantizar una adecuada perfusión tisular.11
En lo que respecta al equilibrio hidrosalino, el volumen plasmático aumenta entre un 40% a 50% (ver figura 1).9 Esto junto a un incremento del 25% en la frecuencia cardiaca y una disminución de la RVP lleva a un aumento del gasto cardiaco que puede ascender hasta un 45% en la semana 24 de gestación.8,10–13
En pacientes con preeclampsia se ha encontrado niveles más bajo de aldosterona, lo que podría sugerir un rol en la angiogénesis placentaria de esta hormona, además de la retención de sodio a nivel tubular.8,11 (ver figura 2).
Patología cardiovascular previa y embarazo
Existen variables que se asocian a desenlaces adversos durante la gestación, como la paridad, edad, peso, dislipidemia, entre otras. Es importante identificar estas condiciones preexistentes debido a que son factores de riesgo para desarrollar trastornos hipertensivos.14,15
Egeland et al, realizaron un estudio de cohorte prospectivo en 13217 gestantes y analizaron múltiples variables preconcepcionales y su asociación con el desarrollo de trastornos hipertensivos en el embarazo.14 (Ver tabla 1).
TRASTORNOS HIPERTENSIVOS EN EL EMBARAZO Y RIESGO CARDIOVASCULAR
Los trastornos hipertensivos del embarazo se mantienen como una de las causas principales de morbimortalidad en las gestantes.16 Acorde a las guías americanas de obstetricia (American College of Obstetrics & Gynecology) los trastornos hipertensivos del embarazo se clasifican según se señalan en la tabla 2.17 La relevancia a futuro de estos trastornos radica en su relación establecida con el riesgo cardiovascular y su impacto en salud y costos.18
Desde el estudio Framingham de 1948 se viene reconociendo la importancia de la hipertensión como un factor crucial en el desarrollo de enfermedades cardiovasculares.19 Asimismo, en 2017 la Asociación Americana del Corazón (AHA) publicó sus guías sobre manejo de la hipertensión, con un radical cambio: reducción en el punto de corte para el diagnóstico, basando esta premisa no en valores absolutos de cifras tensionales, si no en el valor del riesgo cardiovascular asociado.20
Debido a que, de los cuatro trastornos descritos, dos de ellos ya tienen un diagnóstico claro, en esta revisión solo se enfocará lo relacionado a la preeclampsia y la hipertensión gestacional.
Actualmente no existe un modelo que explica por si solo el desarrollo de preeclampsia. Diferentes modelos incluyen disfunción endotelial placentaria que libera a la circulación sistémica factores antiangiogénicos y proinflamatorios21,22. Otro modelo relaciona la presencia de autoanticuerpos dirigidos contra el receptor de angiotensina-II con efecto agonista, que se han demostrado estar presentes durante el puerperio tardío en mujeres con antecedente de preeclampsia, como una posible causa de hipertensión subsecuente23.
En lo que respecta a la hipertensión gestacional, no hay una fisiopatología clara, y se habla de esta como un estadio previo a la preeclampsia con una mejor adaptación materna a los factores inflamatorios.24
Como se reconoció anteriormente, el cálculo del riesgo cardiovascular es fundamental para dirigir el tratamiento. Para esto existen múltiples scores, no obstante, en ninguno de ellos se incluye la población gestante, por lo que no está validado su uso.25 De igual manera, los grandes ensayos clínicos que han guiado la terapia antihipertensiva tampoco han incluido a embarazadas.26 Es así como las definiciones para los trastornos hipertensivos en el embarazo distan notablemente de la población general, y aunque se reconoce que se debe disminuir el punto de corte, esto no ha sucedido.
Con el objetivo de disminuir el desarrollo de preeclampsia, se recomienda clasificar el riesgo de las pacientes de acuerdo a las condiciones descritas en la tabla 3. Adicionalmente se recomienda el inicio de aspirina en quienes cumplan estos criterios a una dosis 100-150 mg/día a partir de la semana 12 hasta la 36-37. 27,28
En el año 2015 se llevó a cabo el estudio CHIPS (Control of Hypertension in Pregnancy Study), el cual evaluó si existían diferencias entre un control estricto vs convencional de presión arterial. Se aleatorizaron 987 mujeres al grupo de control estricto (PAD 85 mmHg) vs convencional (PAD 100 mmHg) y se evaluó el desenlace primario compuesto de pérdidas maternas o cuidado intensivo neonatal mayor a 48 horas. No se encontraron diferencias significativas entre estos dos grupos.29 No obstante, se encontró un mayor riesgo en el grupo convencional para desarrollar hipertensión severa y sus implicaciones cardiovasculares maternas. Entre los fármacos de elección, no hay evidencia sólida si alguno presenta mayor beneficio o menores efectos adversos. Tanto las guías de la AHA como la ACOG recomiendan indistintamente el uso de alfa y beta bloqueadores mixtos o bloqueante de canales de calcio (nifedipino).17
A falta de un score objetivo que permita evaluar el riesgo a 10 años, se han llevado a cabo estudios que miden la incidencia de desenlaces cardiovasculares antes y después de 10 años de seguimiento en pacientes con diagnóstico de preeclampsia/hipertensión gestacional, encontrándose lo siguiente (Tabla 4).30–33
DIABETES GESTACIONAL Y RIESGO CARDIOVASCULAR
La diabetes mellitus gestacional (DMG) es definida como la intolerancia a la glucosa, la cual inicia o es reconocida por primera vez durante la gestación.34 Su prevalencia es muy variable, Europa reporta entre el 2-6% de gestantes, en Estados Unidos se estima entre el 7-18%, para América Latina esta alrededor del 10–33% y en Colombia oscila entre 1,43- 6,3%.35,36
Diagnóstico
La American Diabetes Association (ADA) recomienda realizar una prueba de tolerancia oral a la glucosa de 75g a las 24-28 semanas de gestación. Se hace el diagnóstico si se cumple alguna de las siguientes condiciones:37
- Glucosa en ayunas ≥ 92 mg/dL
- Glucosa posprandial 1h ≥ 180 mg/dL
- Glucosa posprandial 2h ≥ 153 mg/dL
Tratamiento no farmacológico
Después del diagnóstico, el tratamiento comienza con nutrición controlada (dirigida y seguida por nutricionista), actividad física, y control de peso dependiendo del peso pregestacional. Estudios sugieren que con estas medidas casi el 80% de las pacientes con DMG logran metas glicémicas.38
Terapia oral vs inyectable
La recomendación actual indica que el manejo estándar de la DMG debe realizarse con insulinoterapia, sin embargo, esta terapia presenta múltiples desventajas tales como: varias inyecciones al día, riesgo de hipoglicemias y ganancia de peso. Por lo cual recurrir a este tratamiento requiere una guía estricta y detallada para su autocuidado seguro, que muchas veces no se puede garantizar por parte de las pacientes por su nivel socioeconómico, cultural, entre otros. De modo que el cambio a terapia oral subsanaría estas dificultades.39
El uso de metformina en la gestación sigue siendo controvertido debido a que atraviesa la placenta y alcanza concentraciones significativas en cordón umbilical; por tal motivo en la práctica diaria no está sistematizado su uso.32
Gui et al, en el año 2013 comparó el uso de metformina versus insulina para el tratamiento de mujeres con DMG o mujeres embarazadas con diabetes mellitus tipo 2. Encontró resultados comparables en ambos grupos en cuanto a metas glicémicas y desenlaces neonatales. Además la metformina redujo el riesgo de hipoglucemia neonatal RR 0,63; IC del 95% [0.45-0.87 ] e hipertensión inducida por el embarazo RR 0.56, IC 95% [0.37-0.85], y ganancia de peso gestacional reducida (diferencia media -2.07, IC del 95%: [-2.88 a -1.27] en comparación con la terapia con insulina.40
Además, el uso de metformina en el embarazo ha reportado beneficios cardiovasculares adicionales, como prevención en preeclampsia e hipertensión gestacional, aunque esto debe corroborarse con estudios más amplios ya que la evidencia actual solo ha sido en ensayos pequeños sin significación estadística.41
Metas glicémicas
De acuerdo a la ADA y ACOG, una meta de hemoglobina glicada (HbA1c) <6% sería lo ideal, teniendo en cuenta que la anemia fisiológica presente en el embarazo reduce el valor de referencia de esta. No obstante, si existen riesgos de hipoglicemia una meta entre 6.5-7% podría ser benéfico. Para las pacientes insulinorrequirientes se plantean metas en ayunas <95 mg/dL y posprandiales <120 mg/dL.42
Teniendo en cuenta esto, ¿una meta más estricta favorece menores desenlaces cardiovasculares y obstétricos?
Una revisión de Cochrane de 2016 sobre metas glicémicas en DMG, en un pequeño ensayo clínico con 180 pacientes no demostró diferencias significativas en cuanto a metas estrictas vs convencionales y mejores desenlaces maternos (desarrollo de trastornos hipertensivos, parto por cesárea) o fetales (RCIU, macrosomía, bajo peso al nacer).43
Extrapolando otro estudio en gestantes con diabetes mellitus tipo 1 pregestacional, tampoco se encontraron diferencias en desenlaces materno-fetales, pero en el grupo intensivo se reportaron más efectos adversos.44
Es importante señalar que, si se utiliza únicamente la HbA1c como indicador de control metabólico puede resultar poco confiable debido a la anemia fisiológica presente, por lo tanto, se recomienda que las metas terapéuticas se guíen de forma conjunta con la glucosa plasmática en ayunas, especialmente en el segundo y tercer trimestre.45
PAPEL DE LAS ESTATINAS EN EL EMBARAZO
Actualmente las estatinas son categoría X según la FDA, por lo que no se recomienda su uso en el embarazo.46 Sin embargo, estas tienen múltiples efectos benéficos como la antiagregación plaquetaria, modulación de la respuesta inflamatoria y aumento en la actividad de la sintasa de óxido nítrico endotelial. Además, juegan un papel fundamental en el manejo de la enfermedad cardiovascular aterosclerótica, por lo que se intenta incorporar estos beneficios en las gestaciones con alto riesgo cardiovascular. En función de esto existen estudios que buscan replantear la categoría asignada por la FDA.
Karalis et al, realizaron una revisión sistemática con 16 estudios, incluyendo un ensayo clínico controlado aleatorizado y 4 revisiones sistemáticas, cuyos resultados sugieren la ausencia de relación entre el uso de estatinas hidrofílicas y efectos teratogénicos, apuntando a ser seguras durante la gestación.47
Zarek et al, en el año 2014 publicaron un metaanálisis que recopiló 6 estudios de casos y controles. Este buscaba determinar el riesgo de aparición de malformaciones fetales con el uso de estatinas en la población gestante. Encontraron que no había diferencias en la presentación de malformaciones fetales entre el grupo control y el grupo expuesto RR 1,15 IC95% [0.75-1.76]. 48
Debido a la calidad de la evidencia actual se requieren estudios más rigurosos que permitan establecer su uso seguro y sus potenciales beneficios en los embarazos de alto riesgo cardiovascular.
CONCLUSIONES
La relación entre embarazo y riesgo cardiovascular es un hecho importante para tener en cuenta durante la valoración actual y a futuro en la salud de la mujer. La presencia de desenlaces maternos adversos podría considerarse como un equivalente de alto riesgo para el desarrollo de enfermedad cardiovascular aterosclerótica. Se hace imperante la necesidad de una estimación objetiva del riesgo para esta población y de investigar más en nuevas terapias que ayuden a disminuir el riesgo, prevenir dichos eventos y que al mismo tiempo sean seguros durante el embarazo y postparto.
REFERENCIAS
- World Health Organization. Enfermedades cardiovasculares. https://www.who.int/es/news-room/fact-sheets/detail/cardiovascular-diseases-(cvds). Published 2017.
- Brown MC, Best KE, Pearce MS, Waugh J, Robson SC, Bell R. Cardiovascular disease risk in women with pre-eclampsia: Systematic review and meta-analysis. Eur J Epidemiol. 2013;28(1):1-19. doi:10.1007/s10654-013-9762-6
- Shapero KS, Desai NR, Elder RW, Lipkind HS, Chou JC, Spatz ES. Cardio-obstetrics: Recognizing and managing cardiovascular complications of pregnancy. Cleve Clin J Med. 2020;87(1):43-52. doi:10.3949/ccjm.87a.18137
- Wenger NK. Recognizing pregnancy-associated cardiovascular risk factors. Am J Cardiol. 2014;113(2):406-409. doi:10.1016/j.amjcard.2013.08.054
- Lane-Cordova AD, Khan SS, Grobman WA, Greenland P, Shah SJ. Long-Term Cardiovascular Risks Associated With Adverse Pregnancy Outcomes: JACC Review Topic of the Week. J Am Coll Cardiol. 2019;73(16):2106-2116. doi:10.1016/j.jacc.2018.12.092
- Riise HKR, Sulo G, Tell GS, et al. Hypertensive pregnancy disorders increase the risk of maternal cardiovascular disease after adjustment for cardiovascular risk factors. Int J Cardiol. 2019;282(2019):81-87. doi:10.1016/j.ijcard.2019.01.097
- Sanghavi M, Rutherford JD. Cardiovascular physiology of pregnancy. Circulation. 2014;130(12):1003-1008. doi:10.1161/CIRCULATIONAHA.114.009029
- Soma-Pillay P, Nelson-Piercy C, Tolppanen H, Mebazaa A. Physiological changes in pregnancy. Cardiovasc J Afr. 2016;27(2):89-94. doi:10.5830/CVJA-2016-021
- Troiano NH. Physiologic and hemodynamic changes during pregnancy. AACN Adv Crit Care. 2018;29(3):273-283. doi:10.4037/aacnacc2018911
- Iacobaeus C, Andolf E, Thorsell M, Bremme K, Ostlund E, Kahan T. Cardiac function, myocardial mechano-energetic efficiency, and ventricular-arterial coupling in normal pregnancy. J Hypertens. 2018;36(4):857-866. doi:10.1097/HJH.0000000000001612
- Sanghavi M, Rutherford JD. Cardiovascular physiology of pregnancy. Circulation. 2014;130(12):1003-1008. doi:10.1161/CIRCULATIONAHA.114.009029
- Rafik R, Larsson A, Pernow J, Bremme K, Eriksson MJ. Assessment of left ventricular structure and function in preeclampsia by echocardiography and cardiovascular biomarkers. J Hypertens. 2009;21(11):2257-2264. doi:10.1097/HJH.0b013e3283300541
- Ouzounian JG, Elkayam U. Physiologic Changes During Normal Pregnancy and Delivery. Cardiol Clin. 2012;30(3):317-329. doi:10.1016/j.ccl.2012.05.004
- Egeland GM, Klungsøyr K, Øyen N, Tell GS, Næss Ø, Skjærven R. Preconception cardiovascular risk factor differences between gestational hypertension and preeclampsia: Cohort Norway study. Hypertension. 2016;67(6):1173-1180. doi:10.1161/HYPERTENSIONAHA.116.07099
- Dayan N , Lanes A , Walker M, Spitzer K LC. Effect of chronic hypertension on assisted pregnancy outcomes : a population-based study in. Fertil Steril. 2015;105(4):1003-1009. doi:10.1016/j.fertnstert.2015.11.039
- Khan KS, Wojdyla D, Say L, Gülmezoglu AM, Van Look PF. WHO analysis of causes of maternal death: a systematic review. Lancet. 2006;367(9516):1066-1074. doi:10.1016/S0140-6736(06)68397-9
- Gestational hypertension and preeclampsia. ACOG Practice Bulletin No. 202. Am Coll Obstet Gynecol. 2019;44(3):170. doi:10.1097/NMC.0000000000000523
- Stevens W, Shih T, Incerti D, et al. Short-term costs of preeclampsia to the United States health care system. Am J Obstet Gynecol. 2017;217(3):237-248.e16. doi:10.1016/j.ajog.2017.04.032
- Mahmood SS, Levy D, Vasan RS, Wang TJ. The Framingham Heart Study and the epidemiology of cardiovascular disease: A historical perspective. Lancet. 2014;383(9921):999-1008. doi:10.1016/S0140-6736(13)61752-3
- Whelton PK, Carey RM, Aronow WS, Casey Jr DE, Collins KJ, Dennison Himmelfarb C, DePalma SM, Gidding S, Jamerson KA, Jones DW, MacLaughlin EJ, Muntner P, Ovbiagele B, Smith Jr SC, Spencer CC, Stafford RS, Taler SJ, Thomas RJ, Williams Sr KA, Williamson JD WJJ. 2017 Guideline for the Prevention, Detection, Evaluation, and Management of High Blood Pressure in Adults. J Am Coll Cardiol. 2017;70(14):1785-1822. doi:10.1016/j.jacc.2017.07.745
- Kvehaugen AS, Dechend R, Ramstad HB, Troisi R, Fugelseth D, Staff AC. Endothelial function and circulating biomarkers are disturbed in women and children after preeclampsia. Hypertension. 2011;58(1):63-69. doi:10.1161/HYPERTENSIONAHA.111.172387
- Sánchez-Aranguren LC, Prada CE, Riaño-Medina CE, Lopez M. Endothelial dysfunction and preeclampsia: Role of oxidative stress. Front Physiol. 2014;5:1-11. doi:10.3389/fphys.2014.00372
- Xia Y, Kellems RE. Angiotensin receptor agonistic autoantibodies and hypertension : Preeclampsia and beyond. Circ Res. 2013;113(1):78-87. doi:10.1161/CIRCRESAHA.113.300752
- Tangerås LH, Austdal M, Skråstad RB, et al. Distinct First Trimester Cytokine Profiles for Gestational Hypertension and Preeclampsia. Arterioscler Thromb Vasc Biol. 2015;35(11):2478-2485. doi:10.1161/ATVBAHA.115.305817
- Stuart JJ, Tanz LJ, Cook NR, et al. Hypertensive Disorders of Pregnancy and 10-Year Cardiovascular Risk Prediction. J Am Coll Cardiol. 2018;72(11):1252-1263. doi:10.1016/j.jacc.2018.05.077
- Food and Drug Administration. Pregnant Women: Scientific and Ethical Considerations for Inclusion in Clinical Trials Guidance for Industry. 2018;4(April 2018):1-14. https://www.fda.gov/Drugs/GuidanceComplianceRegulatoryInformation/Guidances/default.htm%0Ahttp://www.fda.gov/BiologicsBloodVaccines/GuidanceComplianceRegulatoryInformation/Guidances/default.htm.
- Regitz-Zagrosek V, Roos-Hesselink JW, Bauersachs J, et al. 2018 ESC Guidelines for the management of cardiovascular diseases during pregnancy. Eur Heart J. 2018;39(34):3165-3241. doi:10.1093/eurheartj/ehy340
- Bartsch E, Medcalf KE, Park AL, et al. Clinical risk factors for pre-eclampsia determined in early pregnancy: Systematic review and meta-analysis of large cohort studies. BMJ. 2016;353:i1753. doi:10.1136/bmj.i1753
- Goyal M, Demchuk AM, Hill MD. Less-Tight versus Tight Control of Hypertension in Pregnancy. N Engl J Med. 2015;372:2366-2368. doi:10.1056/NEJMc1504715
- Riise HKR, Sulo G, Tell GS, et al. Incident coronary heart disease after Preeclampsia: Role of reduced fetal growth, preterm delivery, and parity. J Am Heart Assoc. 2017;6(3):1-13. doi:10.1161/JAHA.116.004158
- Cirillo PM, Cohn BA. Pregnancy complications and cardiovascular disease death 50-year follow-up of the child health and development studies pregnancy cohort. Circulation. 2015;132(13):1234-1242. doi:10.1161/CIRCULATIONAHA.113.003901
- Kristensen JH, Basit S, Wohlfahrt J, Damholt MB, Boyd HA. Pre-eclampsia and risk of later kidney disease: Nationwide cohort study. Br Med J. 2019;365(3):1-9. doi:10.1136/bmj.l1516
- Ying W, Catov JM, Ouyang P. Hypertensive disorders of pregnancy and future maternal cardiovascular risk. J Am Heart Assoc. 2018;7(17):1-9. doi:10.1161/JAHA.118.009382
- Baz B, Riveline JP, Gautier JF. Gestational diabetes mellitus: Definition, aetiological and clinical aspects. Eur J Endocrinol. 2016;174(2):R43-R51. doi:10.1530/EJE-15-0378
- Buckley BS, Harreiter J, Damm P, et al. Gestational diabetes mellitus in Europe: Prevalence, current screening practice and barriers to screening. A review. Diabet Med. 2012;29(7):844-854. doi:10.1111/j.1464-5491.2011.03541.x
- Ruiz-Hoyos BM, Londoño-Franco Ángela L R-AR. Prevalencia de Diabetes Mellitus Gestacional por curva de tolerancia a la glucosa en semanas 24 a 28. Cohorte prospectiva en Armenia Colombia, 2015-2016. Rev Colomb Obs Ginecol. 2018;69(2):108-116. https://revista.fecolsog.org/index.php/rcog/article/view/3056.
- American Diabetes Association. 6.Glycemic Targets: Standards of Medical Care in Diabetes-2020. Diabetes Care. 2020;43(1):S66-S76. doi:10.2337/dc20-S006
- Verc¸oza Viana L, Gross JL, Azevedo MJ. Dietary intervention in patients with gestational diabetes mellitus: A systematic review and meta-analysis of randomized clinical trials on maternal and newborn outcomes. Diabetes Care. 2014;37(12):3345-3355. doi:10.2337/dc14-1530
- Poomalar GK. Changing trends in management of gestational diabetes mellitus. World J Diabetes. 2015;6(2):284. doi:10.4239/wjd.v6.i2.284
- Gui J, Liu Q, Feng L. Metformin vs Insulin in the Management of Gestational Diabetes: A Meta-Analysis. PLoS One. 2013;8(5):1-8. doi:10.1371/journal.pone.0064585
- Kalafat E, Sukur YE, Abdi A, Thilaganathan B, Khalil A. Metformin for prevention of hypertensive disorders of pregnancy in women with gestational diabetes or obesity: systematic review and meta-analysis of randomized trials. Ultrasound Obstet Gynecol. 2018;52(6):706-714. doi:10.1002/uog.19084
- American Diabetes Association. 14. Management of Diabetes in Pregnancy: Standards of Medical Care in Diabetes-2020. Diabetes Care. 2020;43(1):S183-S192. doi:10.2337/dc20-S014
- Martis R, Brown J, Alsweiler J, Crawford TJ, Crowther CA. Different intensities of glycaemic control for women with gestational diabetes mellitus. Cochrane database Syst Rev. 2016;4(4):CD011624. doi:10.1002/14651858.CD011624.pub2
- Middleton P, Crowther CA, Simmonds L. Different intensities of glycaemic control for pregnant women with pre-existing diabetes. Cochrane Database Syst Rev. 2016;2016(5):58. doi:10.1002/14651858.CD008540.pub4
- National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. NICE Guidel. 2015;63(2008):42.
- Kusters DM, Lahsinoui HH, Van De Post JAM, et al. Statin use during pregnancy: A systematic review and meta-analysis. Expert Rev Cardiovasc Ther. 2012;10(3):363-378. doi:10.1586/erc.11.196
- Karalis DG, Hill AN, Clifton S, Wild RA. The risks of statin use in pregnancy: A systematic review. J Clin Lipidol. 2016;10(5):1081-1090. doi:10.1016/j.jacl.2016.07.002
- Zarek J, Koren G. Motherisk rounds: The Fetal Safety of Statins: A Systematic Review Meta-Analysis. J Obstet Gynaecol Canada. 2014;36(6):506-509. doi:10.1016/S1701-2163(15)30565
TABLAS Y FIGURAS
| Tabla 1. Factores de riesgos para desarrollar trastornos hipertensivos en el embarazo | ||||
| Hipertensión gestacional OR (IC 95%) | Preeclampsia OR (IC 95%) | Preeclampsia pretérmino OR (IC 95%) | Preecampsia a término OR (IC 95%) | |
| Hipertensión arterial | – | 3.5 (2.48–4.97) | 3.8 (2.04–7.08) | 3.4 (2.32–5.01) |
| IMC 25 – 29.9 | 1.8 (1.31–2.56) | 1.7 (1.32–2.18) | 1.2 (0.69–1.92) | 1.9 (1.46–2.52) |
| IMC >30 | 4.2 (2.86–6.21) | 2.0 (1.35–3.02) | 2.2 (1.13–4.09) | 2.0 (1.21–3.14) |
| Hipercolesterolemia | 1.9 (1.11–3.10) | 1.8 (1.17–2.84) | 2.4 (1.24–4.65) | 1.6 (0.94–2.85) |
| Hipertrigliceridemia | 1.3 (0.84–2.03) | 2.4 (1.71–3.30) | 2.3 (1.29–4.07) | 2.4 (1.65–3.52) |
| Nota. Adaptado de Effect of chronic hypertension on assisted pregnancy outcomes : a population-based study in. Fertil Steril. 14 | ||||
| Tabla 2. Clasificación de los trastornos hipertensivo del embarazo. | |
| Trastorno hipertensivo | Definición |
| Preeclampsia | Elevación de la presión arterial ≥ 140/90 mmHg después de 20 semanas acompañado de proteinuria o disfunción de órgano blanco.
|
| Hipertensión gestacional | Elevación de la presión arterial ≥ 140/90 mmHg después de 20 semanas sin datos de disfunción de órgano blanco.
|
| Hipertensión crónica | Presión arterial elevada antes de 20 semanas o después de 12 semanas posparto.
|
| Hipertensión crónica con preeclampsia sobreagregada | Presión arterial elevada previamente documentada con aparición de novo de proteinuria o disfunción de órgano blanco. |
| Nota. Fuente: Gestational hypertension and preeclampsia. ACOG Practice Bulletin No. 202. 17 | |
| Tabla 3. Características clínicas asociadas al desarrollo de preeclampsia | |
| Alto riesgo (Cualquiera de los siguientes) | Moderado riesgo (dos o más) |
| Trastorno hipertensivo en embarazo previo | Primer embarazo |
| Enfermedad renal crónica | Edad mayor a 40 años |
| Enfermedad autoinmune (LES o Síndrome Antifosfolípido)
|
Periodo intergenésico mayor a 10 años |
| Diabetes Mellitus tipo 1 o 2 | IMC > 35 al ingreso del control prenatal |
| Hipertensión arterial crónica | Multigestante |
|
Nota. Adaptado de Clinical risk factors for pre-eclampsia determined in early pregnancy: Systematic review and meta-analysis of large cohort studies28
|
|
| Tabla 4. Incidencia de desenlaces cardiovasculares en preeclampsia/hipertensión gestacional | |||
| Seguimiento | Trastorno | Hipertensión gestacional | Preeclampsia |
| <10 años | RCV | ++ | ++ |
| HTA | +++ | +++ | |
| ERC | + | ++ | |
| >10 años | RCV | + | ++ |
| HTA | +++ | +++ | |
| Enfermedad Coronaria | + | ++ | |
| ACV | + | + | |
| FC | + | + | |
| ERC | + | + | |
| Muerte | + | ++ | |
| Nota. Fuente: adaptado de Hypertensive Disorders of Pregnancy and Future Maternal Cardiovascular Risk33
RCV: Riesgo cardiovascular, HTA: Hipertensión arterial, ERC: Enfermedad renal crónica, ACV: Accidente cerebrovascular, FC: Falla cardiaca. +: Riesgo aumentado levemente (HR<2) ++: Riesgo aumentado moderadamente (HR>2), +++ Riesgo marcadamente aumentado (HR>3)
|
|||
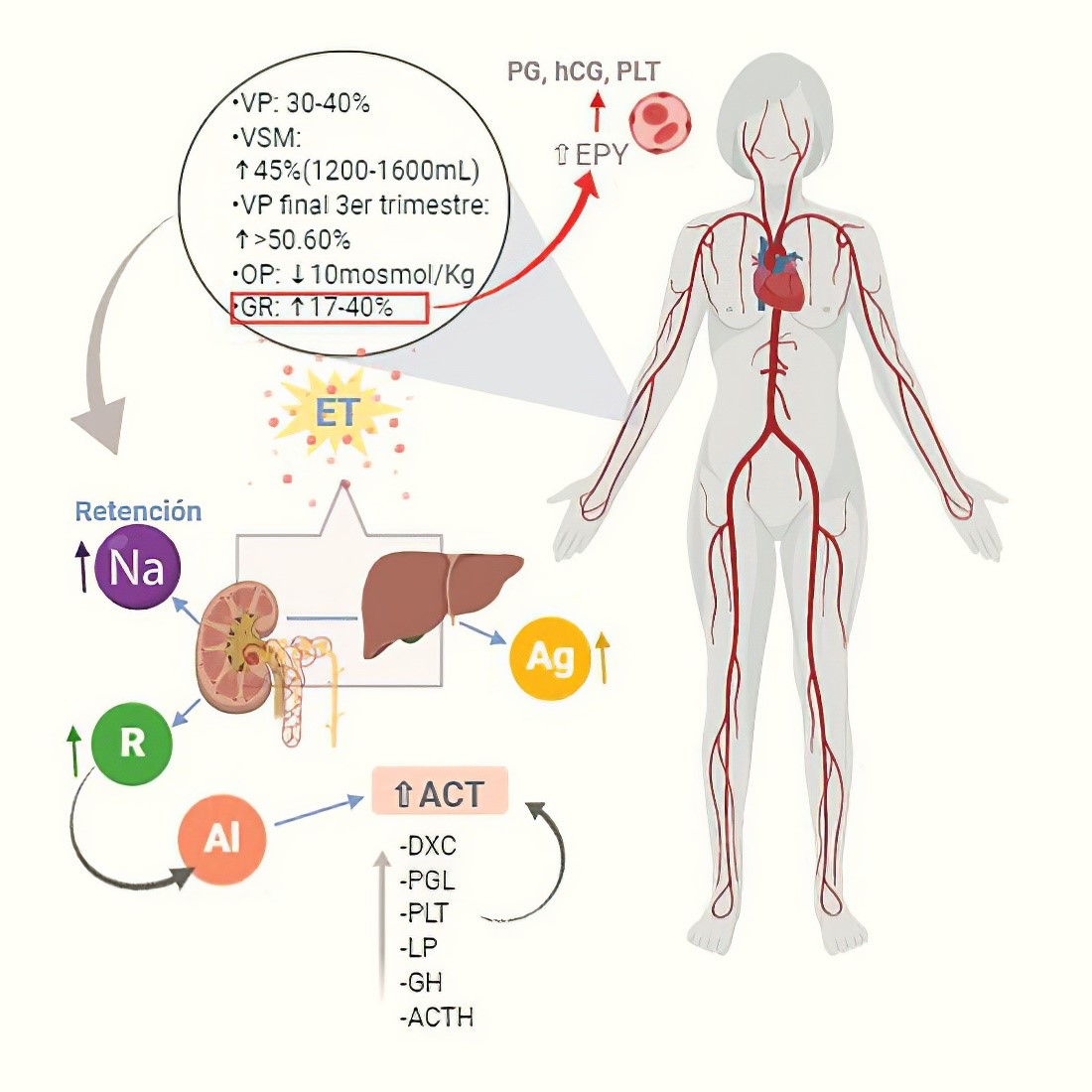
Figura 1. Mecanismos del aumento de la volemia en el embarazo
ET:estrógenos, VP:volumen plasmático, VSM: volumen sanguíneo materno, OP: osmolalidad plasmática, GR: glóbulos rojos, Na: sodio, R: renina, Al: aldosterona, Ag: angiotensinógeno, ACT: agua corporal total, PG: progesterona, PLT: prolactina, EPY: eritropoyesis, DXC: desoxicorticosterona, PGL: prostaglandinas, LP: lactógeno placentario, GH: hormona del crecimiento, ACTH: adrenocorticotropina.
Durante el período de gestación, el estado hipervolémico es producto de cambios fisiológicos provenientes de diversos mecanismos que aún no son totalmente claros. El estrógeno cumple una función relevante en mencionado proceso, promueve la producción de renina renal en las células yuxtaglomerulaes, aumeta la producción de angiotensinógeno, sustrato de la renina, por parte del hígado, la renina a su vez estimula la producción de aldosterona y en conjunto, se eleva la retención de Na y agua resultando en incremento de la volemia. Existen otras hormonas que contribuyen a la hipervolemia como, las prostaglandinas, la prolactina, la hormona del crecimiento, la hormona adrenocorticotrófica, la desoxicorticosterona y el lactógeno placentario. 8,13
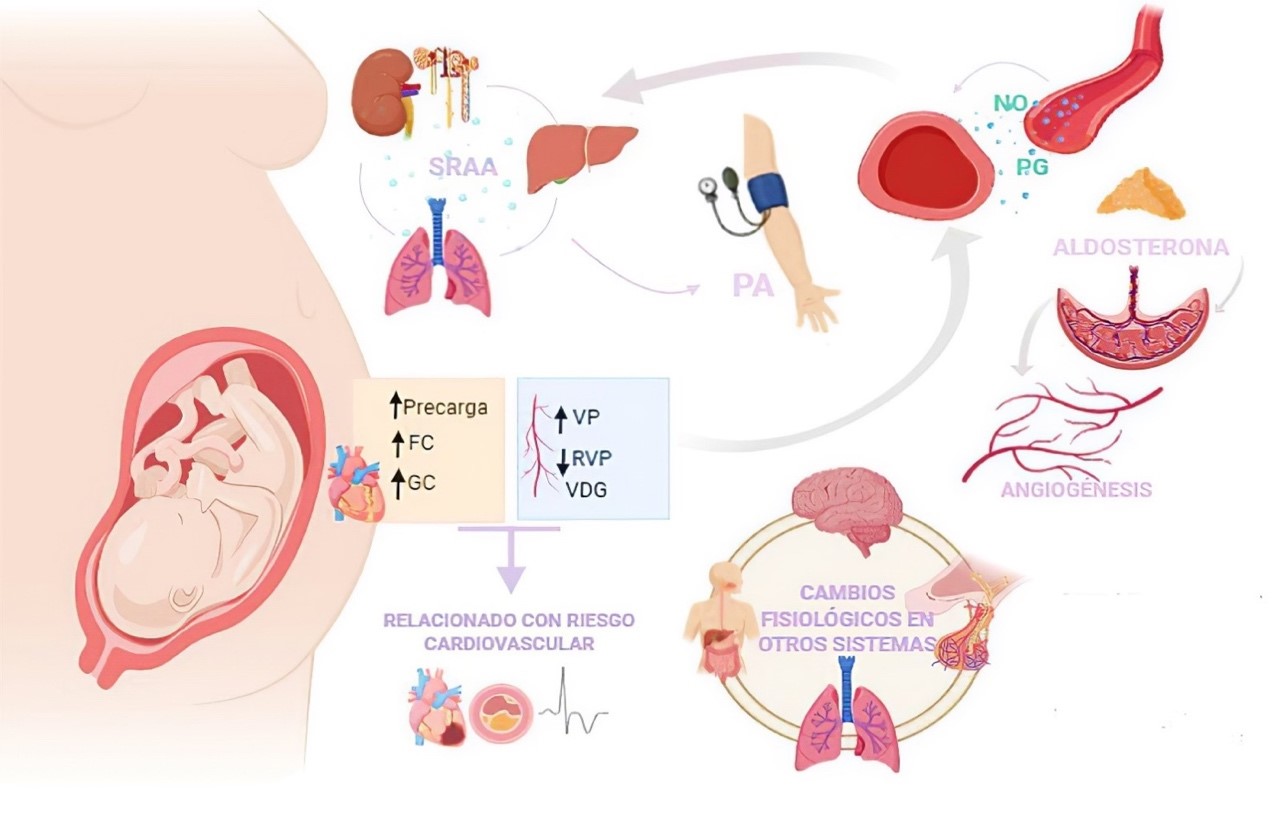
Figura 2. Cambios fisiológicos cardiovasculares durante el embarazo. FC: frecuencia cardíaca, GC: gasto cardíaco, VP: volumen plasmático, RVP: resistencia vascular periférica, VDG: vasodilatación generalizada, SRAA: sistema renina angiotensina aldosterona, PA: presión arterial, NO: óxido nítrico; PG, progesterona.8,11



