2019
2
Autores:
Eduardo Reyna-Villasmil, Jorly Mejia-Montilla, Nadia Reyna-Villasmil, Duly Torres-Cepeda, Marta Rondón-Tapía, Andreina Fernández-Ramírez, Carlos Briceño-Pérez
Tipo de documento:
Artículo de investigaciónFUROSEMIDA EN EL CONTROL DE LA HIPERTENSIÓN ARTERIAL POSPARTO EN PREECLÁMPTICAS SEVERAS
Contenido del documento:
RESUMEN
OBJETIVO: Establecer la utilidad de la furosemida en el control de la hipertensión arterial posparto en preeclámpticas severa. MÉTODOS: Se realizó un estudio de casos y controles en el Hospital Central “Dr. Urquinaona”, Maracaibo, Venezuela. Se incluyeron pacientes con preeclampsia severa, las cuales durante el posparto fueron asignadas al azar para ser tratadas con furosemida, alfametildopa y cloruro de potasio oral (grupo A) o alfa-metildopa oral (grupo B) por 48 horas. Los parámetros evaluados fueron: variaciones en los valores de presión arterial y frecuencia cardiaca, persistencia de hipertensión, parámetros de laboratorio y efectos adversos. RESULTADOS: Para el análisis final estaban disponibles los datos de 198 pacientes en el grupo A y 197 pacientes en el grupo B en cada uno de los grupos. Luego de 48 horas de tratamiento se observaron disminuciones estadísticamente significativas en los valores de presión arterial sistólica y diastólica entre las pacientes tratadas con furosemida y las pacientes del grupo control (p < 0,0001). Se observó persistencia de la hipertensión en 52 pacientes (26,3 %) del grupo A y en 134 pacientes (68,0 %) del grupo B (p < 0,0001). No se encontraron diferencias entre los grupos en la frecuencia cardiaca, valores de laboratorio y efectos adversos (p = ns). CONCLUSIÓN: La furosemida produce disminuciones significativas en los valores promedios de presión arterial sistólica y diastólica, al igual que en la frecuencia de persistencia de hipertensión postparto en preeclámpticas severas.
PALABRAS CLAVE: Furosemida; Diuréticos; Preeclampsia severa; Hipertensión; Posparto
SUMMARY
OBJECTIVE: To establish the utility of furosemide in the control of postpartum blood pressure in severe preeclamptic patients. METHODS: A case-control study was conducted at the Central Hospital «Dr. Urquinaona», Maracaibo, Venezuela. Patients diagnosed with severe preeclampsia were included, who during the postpartum period were randomized to be treated with furosemide, alpha-methyldopa and oral potassium chloride (group A) or oral alpha-methyldopa (group B) for 48 hours. The parameters evaluated were: variations in blood pressure and heart rate values, the persistence of hypertension, laboratory parameters and adverse effects related to treatment. RESULTS: Data of 198 patients in group A and 197 patients in group B in each of the groups were available for the final analysis. After 48 hours of treatment, statistical significant decreases were observed in the values of systolic and diastolic blood pressure between patients treated with furosemide and patients in the control group (p <0.0001). Persistence of hypertension was observed in 52 patients (26.3 %) of group A and in 134 patients (68.0 %) of group B (p < 0.0001). No differences were found between the groups in heart rate, laboratory values and adverse effects (p = ns). CONCLUSION: Furosemide produces significant decreases in the mean values of systolic and diastolic blood pressure, as well as in the frequency of persistence of postpartum hypertension in severe preeclamptic patients.
KEY WORDS: Furosemide; Diuretics; Severe preeclampsia; Hypertension; Postpartum.
INTRODUCCIÓN
Los preeclampsia es una de las principales causas de morbi-mortalidad materna 1,2. No obstante, existe poca información sobre la mejor forma de control y tratamiento de la hipertensión posparto, independientemente del tipo o gravedad. La presión arterial aumenta durante los primeros cinco días del puerperio, alcanzando su punto máximo 3-6 días después del parto 3-5. Se considera que este patrón es secundario a la movilización de líquidos corporales del espacio extravascular al intravascular (de seis a ocho litros de agua corporal total) y de 950 mEq de sodio corporal total acumulados durante el embarazo 6.
La hipertensión posparto puede representar la continuación del trastorno hipertensivo prenatal (independientemente del tipo) o aparecer de novo durante el puerperio. Aunque se reconoce que la hipertensión puede continuar en el posparto, la incidencia y duración con la que esto ocurre ha sido pobremente definida 4. La verdadera prevalencia de hipertensión posparto es difícil de determinar y se relaciona con enfermedades cerebrovasculares y, posiblemente, eclampsia 7.
Hasta el momento no existe una guía única para el manejo para la hipertensión posparto, lo cual condiciona estrategias de manejo en su mayoría incorrectas. Con base en la fisiopatología de la preeclampsia durante el puerperio, parte del tratamiento incluye suspender el uso de analgésicos no esteroideos, sustituyéndolos por fármacos que no afecten las prostaglandinas renales para lograr un manejo adecuado del dolor, obteniendo resultados satisfactorios 8. En otros casos serán necesarios fármacos que permitan lograr un balance hídrico neutro en pacientes que presentan sobrecarga de volumen y el empleo de tratamientos antihipertensivos que pueden ser utilizadas por cortos periodos 9.
Se han propuesto diferentes intervenciones para acelerar la recuperación de las preeclámpticas durante el posparto, pero la efectividad de estos tratamientos, al igual que el tratamiento antihipertensivo ideal, aún debe ser investigada. Las preeclámpticas severas pueden experimentar persistencia de la hipertensión después del parto, secundaria al exceso de agua corporal total y secreción inadecuada de sodio producto de la disminución de la filtración glomerular 10,11. Los diuréticos de asa, como la furosemida, pueden actuar en la sobrecarga hídrica, eliminando el líquido extravascular movilizado durante el puerperio, disminuyendo el volumen sanguíneo y la necesidad del uso de antihipertensivos 6. Al mismo tiempo se logra mantener la presión de llenado capilar pulmonar y aumentar en forma indirecta la presión oncótica, evitando el desarrollo de edema de pulmón e insuficiencia cardiaca congestiva 12.
En la actualidad se conocen pocos datos confiables sobre el manejo de las pacientes con hipertensión posparto con diuréticos y, de igual forma, se desconoce su perfil de eficacia y seguridad, por lo que el objetivo de la investigación fue establecer la utilidad de la furosemida en el control de la hipertensión arterial posparto en preeclámpticas severa.
MÉTODOS
La investigación se realizó entre enero de 2013 y diciembre de 2018 e incluyó embarazadas con diagnóstico de preeclampsia severa que fueron atendidas en el Hospital Central “Dr. Urquinaona”, Maracaibo, Venezuela. La investigación fue aprobada por el Comité de Ética e Investigación del hospital y se obtuvo consentimiento por escrito de todas las participantes.
El tamaño de la muestra se estimó usando la fórmula estadística para contrastar dos promedios. La diferencia esperada en los promedios de presión sanguínea entre los grupos se tomó como 10 mm de Hg. El tamaño de la muestra se estimó en 225 sujetos por cada grupo con un nivel de significancia del 5 % y potencia de 90 %. Se seleccionaron preeclámpticas severas que fueron asignadas al azar para ser tratadas con furosemida (grupo A) o asignadas al grupo control (grupo B). Para obtener una distribución igual en cada grupo, se asignaron sobres sellados que fue abierto por personal externo a la investigación. Esa asignación a cada grupo se realizó una lista aleatoria de números generados por computadora para que la farmacia preparara paquetes que contenían alfametildopa – cloruro de potasio con o sin furosemida, ambos en presentación idéntica, etiquetados con el número de la lista. Se siguió este procedimiento para garantizar el desconocimiento de asignación por las pacientes en cada grupo. La medicación fue empacada y enviada al personal responsable del tratamiento que también era independiente a la investigación.
Se excluyó a las embarazadas con desprendimiento prematuro de placenta, síndrome de HELLP, gestación múltiple, presencia de infección intrauterina o materna activa, enfermedad hipertensiva crónica (hipertensión antes de las 20 semanas de embarazo), enfermedad cardiaca, hematológicas, hepática, renal o sistémica crónica, anemia falciforme, diabetes mellitus pre o gestacional, concentraciones séricas de potasio menor de 3 mEq/L al momento de la selección, antecedentes de consumo de diuréticos o suplementos de potasio, inestabilidad hemodinámica periparto, aquellas embarazadas en las cuales no se pudo realizar el seguimiento u obtener muestras de sangre y con contraindicaciones para el uso de furosemida. También se excluyó a las pacientes que se negaron a participar en la investigación.
La preeclampsia se definió como presión arterial sistólica de 140 mm de Hg o más, o presión arterial diastólica de 90 mm de Hg o más, confirmada por 6 horas o más de diferencia. La proteinuria se definió como 300 mg o más de proteína en una muestra de 48 horas, o 1 a 2 cruces de proteinuria en un examen cualitativo después de las 20 semanas de gestación. Las mediciones de presión sanguínea se realizaron en posición sentada después de 15 minutos de descanso, usando un esfigmógrafo de mercurio estándar con manguito de 14 centímetros. La presión arterial sistólica y diastólica (tomada en relación con el quinto ruido de Korotkoff) se ubicó con relación al punto de 2 mm de Hg más cercano. El método palpatorio se utilizó para verificar las lecturas auscultatorias de la presión arterial sistólica. Las presiones arteriales sistólica y diastólica se calcularon del promedio de la presión arterial de cada brazo.
Antes del inicio de la investigación se realizó un examen físico en el cual se evaluó edad materna, edad gestacional al momento del parto, peso, talla, índice de masa corporal, presión arterial y frecuencia cardiaca. Las pacientes en el grupo A iniciaron el tratamiento con una dosis de furosemida oral (40 mg) junto con 250 mg de alfametildopa cada 6 horas y 1 gramo de cloruro de potasio luego de suspender el tratamiento con sulfato de magnesio endovenoso y del inicio de la diuresis espontanea (más de 50 mL/hora por dos horas consecutivas sin estimulo) durante la hospitalización y antes del alta. Las pacientes del grupo B solo recibieron alfametildopa. Durante el periodo de estudio, no se limitaron las actividades de las pacientes en ambos grupos.
Para la medición de los parámetros de laboratorio se recolectaron 10 mL de sangre de la vena antecubital en todas las pacientes antes la asignación a cada grupo y 48 horas después de del parto. Estas muestras se colocaron en un tubo de vidrio seco, estéril y almacenado a temperatura ambiente y protegidos de la luz ultravioleta. Posteriormente fueron centrifugados a 1600 rpm por 10 minutos y separados en alícuotas y almacenadas a -70º C hasta el momento del análisis.
Las mediciones de hemoglobina y plaquetas se realizaron utilizando un analizador cuantitativo automático de hematología LH75 (Beckman Coulter Inc®, EE.UU.). Las concentraciones séricas de y creatinina también se determinaron por espectrofotometría con un kit comercial (DiaSys Diagnostic Systems®, Alemania) con una sensibilidad de y 0.1 mg/dL. Las concentraciones de transaminasa glutamico-oxalacetica y transaminasa glutamato-piruvica se midieron por el método de espectofotometría usando kits comerciales (DiaSys Diagnostic Systems®, Alemania) con sensibilidad de 4 UI/L y 2 UI/L, respectivamente. Las determinaciones de las concentraciones séricas de deshidrogenasa láctica se realizaron con una prueba comercial cuantitativa, usando una prueba enzimática de lactato a piruvato (Roche Diagnostics Corp®, EE.UU.). Los valores de referencia para cada prueba fue: aspartato aminotransferasa 10 a 40 UI/L, alanino aminotransferasa 10 a 45 UI/L, y deshidrogenasa láctica 300 a 600 U/L. Los coeficientes de variación inter e intraensayo fueron menores del 8 % y 10 %.
Las pacientes de ambos grupos recibieron vigilancia posparto similar, incluida la presión arterial y pulso, medición del peso y diuresis Durante la duración del estudio, se realizó el monitoreo electrónico de la presión arterial en forma discontinua. Los parámetros hemodinámicos se midieron en forma inicial cada 30 minutos en las cuatro primeras horas después de la asignación a cada grupo y posteriormente cada cuatro horas. Si se presentaba algún caso de alteración hemodinámica de cualquier tipo, la paciente era excluida de la investigación y se tomaron las medidas adecuadas para el tratamiento de acuerdo al médico tratante. También se analizaron en cada grupo otros efectos adversos que fueron evaluados por un miembro del grupo que desconocía que tratamiento había recibido la paciente.
Los datos se presentan como valores absolutos y relativos. Para comprobar la distribución normal delos datos se utilizó la prueba de Kolmogorov-Smirnov. El análisis estadístico entre los dos grupos se realizó con la prueba t de Student para datos no relacionados, de manera de comparar las características demográficas, valores de presión arterial, frecuencia cardiaca y parámetros de laboratorio. Los datos cualitativos de la persistencia de hipertensión y frecuencia de efectos adversos fueron analizados con la prueba exacta de Fischer para calcular el riesgo relativo (RR), y el número necesario de tratar entre los grupos y el intervalo de confianza del 95 % (IC 95 %) para cada una de las variables cualitativas de las resultantes estudiadas. Se fijó la significancia estadística en p < 0.05.
RESULTADOS
Se seleccionaron 450 pacientes preeclámpticas severas (225 en el grupo A y 225 en el grupo B) seleccionadas se excluyeron del análisis 11 pacientes del grupo A y 17 pacientes del grupo B, porque durante el periodo de estudio tuvieron que ser tratadas con más de dos antihipertensivos. También, se eliminaron del análisis 27 pacientes (16 pacientes del grupo A y 11 pacientes en el grupo B) por carecer de datos clínicos o de laboratorios completos durante el tratamiento. En total, para el análisis final estaban disponibles los datos de 198 pacientes en el grupo A y 197 pacientes en el grupo B en cada uno de los grupos.
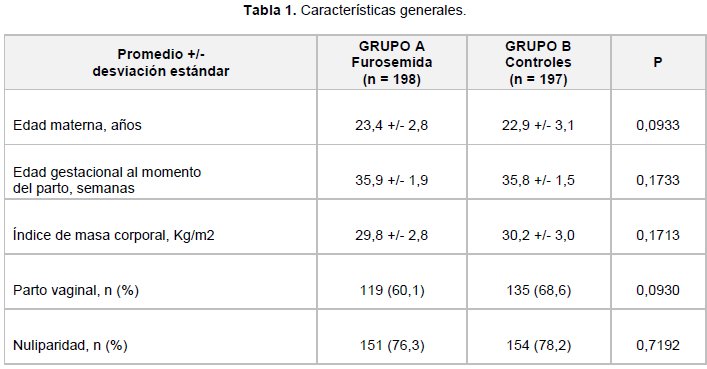
En la tabla 1 se muestran las características generales de ambos grupos de pacientes al inicio del estudio. No se encontraron diferencias entre los grupos con relación a la edad, edad gestacional al momento del parto y el índice de masa corporal (p = ns). Tampoco se observaron diferencias estadísticamente significativas en la frecuencia de parto vaginal y de nuliparidad entre ambos grupos (p = ns).
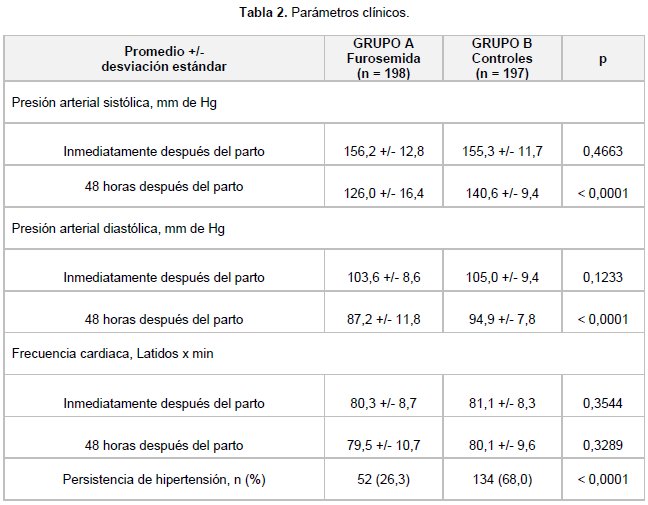
En la tabla 2 se muestran las variables clínicas analizadas en ambos grupos. No se encontraron diferencias estadísticamente significativas en la presión arterial sistólica, presión arterial diastólica y frecuencia cardiaca entre ambos grupos inmediatamente después del parto (p = ns). No obstante, luego de 48 horas se observaron disminuciones estadísticamente significativas en los valores de presión arterial sistólica (126,0 +/- 12,8 mm de Hg para el grupo A comparado con 140,6 +/- 9,4 mm de Hg para el grupo B; p < 0,0001), presión arterial diastólica (87,2 +/- 11,8 mm de Hg para el grupo A comparado con 94,9 mm de Hg para el grupo B; p < 0,0001) entre las pacientes tratadas con furosemida y las pacientes del grupo control. No se encontraron diferencias estadísticamente significativas en los valores de frecuencia cardiaca (p = 0,3289). Se observó persistencia de la hipertensión en 52 pacientes (26,3 %) del grupo A y en 134 pacientes (68,0 %) del grupo B (p < 0,0001). Las pacientes tenían RR de 0,400 (IC 95 %; 0,312 – 0,512). El número de pacientes necesarios de tratar es de 2,39 (IC 95 %; 1,97 – 3,05).
En la tabla 3 se muestran los valores de los parámetros de laboratorio inmediatamente y luego de 48 horas del parto. No se encontraron diferencias significativas en los valores de hemoglobina, plaquetas, creatinina, urea, transaminasas y deshidrogenasa láctica (p = ns).
En ambos grupos el efecto adverso más común fue la cefalea (tabla 4). Sin embargo, no se encontró diferencia estadísticamente significativa entre los grupos (p = 0,5004). Otros efectos adversos como náuseas y vómitos también fueron frecuentes en ambos grupos, pero tampoco mostraron diferencias estadísticamente significativas (p = 0,5435 y p = 0,8102, respectivamente. El resto de los efectos adversos tampoco mostraron diferencias significativas entre los grupos (p = ns).
DISCUSIÓN
Los resultados de la investigación demuestran que el uso de furosemida en preeclámpticas severas permite un mejor control de la hipertensión posparto, ya que disminuye en forma significativa los valores de presión arterial sistólica y diastólica, al igual que la persistencia de hipertensión, sin alterar los parámetros de laboratorio. Estos resultados aportan evidencia sobre la utilidad del uso de furosemida, como tratamiento con ventajas clínicas a otros esquemas de tratamiento tradicionales.
La fisiopatología de la preeclampsia incluye vasoespasmo difuso con daño endotelial 13. La pérdida de proteínas plasmáticas por la endoteliosis glomerular produce disminución de las concentraciones séricas de albumina y globulinas, disminución de la presión oncótica intravascular, escape de líquidos hacia el intersticio y espacio extravascular, resultando en reducción del volumen intravascular y edema sistémico 14,15. Durante el puerperio, este líquido extravascular regresa, produciendo aumento de volumen dentro del compartimento intravascular 16. En algunos casos, la presión oncótica disminuye mientras aumenta la presión venosa central y capilar pulmonar, lo cual favorecen el desarrollo de edema pulmonar, especialmente en las preeclámpticas severas 17,18. El uso prolongado de sulfato de magnesio endovenoso puede agravar todo este proceso y conducir a la aparición de estas complicaciones 19.
Existe escasa evidencia sobre el uso de diuréticos en preeclámpticas. En un estudio realizado por Ascarelli et al. 10 en preeclámpticas severas que recibieron dosis de 20 mg de furosemida durante 5 días el período posparto mejoró la recuperación del paciente al disminuir la presión arterial y la demanda de fármacos antihipertensivos. En otro ensayo en 19 pacientes con diagnóstico de preeclampsia severa que recibieron 40 mg de furosemida o placebo inmediatamente después del parto, se registraron diferencias significativas entre ambos grupos con relación a los valores de presión arterial y persistencia de la hipertensión posparto 20. Se encontró cambios en la presión arterial los días uno, tres y siete después del parto (-6.5 mm de Hg comparado con -3.5 mm de Hg el primer día, -10.6 mm de Hg comparado con -9.75 mm de Hg el tercer día, y -11.5 mm de Hg y -7.8 mm de Hg luego de 7 días de tratamiento en el grupo tratado con furosemida o el grupo placebo, respectivamente). En esta investigación se logró una disminución mayor de la presión arterial, alrededor de 15 mm de Hg en el grupo de pacientes del grupo A, mientras que en el grupo B se observó disminución alrededor de 11 mm de Hg.
Contrario a lo previamente expuesto, otro estudio no encontró diferencias significativas en la presión arterial sistólica y diastólica entre las preeclámpticas que recibieron furosemida comparado con aquellas que recibieron furosemida más nifedipina 21. La posible explicación para este hallazgo es la diferencia en el uso del antihipertensivo que se comenzó a usar tiempo después del inicio de la furosemida para evitar complicaciones relacionadas a la hipertensión.
El edema pulmonar y la insuficiencia cardíaca congestiva posparto pueden ocurrir como resultado del proceso de movilización de líquidos extravasculares, el tratamiento lógico sería utilizar un fármaco que permita mantener la presión venosa central y capilar pulmonar baja e intentar aumentar la presión oncótica para impedir la aparición de las complicaciones 17,22. La restricción de líquidos en el puerperio, junto con la administración de diuréticos, puede considerarse apropiada en circunstancias específicas. Este tratamiento también puede disminuir el riesgo de alteraciones del sistema nervioso central en preeclámpticas severas durante el puerperio, ya que tanto el edema cerebral como la eclampsia posparto, que están íntimamente relacionados con la perfusión cerebral 23,24, podrían evitarse con la disminución del líquido intravascular y del tono venoso periférico 25,26. Los riesgos del tratamiento con diuréticos posparto son escasos y se ha comprobado que disminuyen aún más con el uso de suplemento de potasio oral 21.
El beneficio potencial del uso de diuréticos en las preeclámpticas severas es un tema importante en la obstetricia y medicina materno-fetal contemporánea. Los pacientes con manifestaciones severas de preeclampsia sufren hipertensión marcada y en muchas ocasiones la tarea de controlar la hipertensión arterial posparto asociada a sobrecarga de volumen puede ser difícil. Los resultados de esta investigación demuestran que la persistencia de hipertensión en el posparto es menor en las preeclámpticas severas que recibieron furosemida comparado con el grupo de pacientes que no lo recibieron. Este estudio también demuestra que existen diferencias estadísticamente significativas entre los grupos con relación a los valores de presión arterial sistólica y diastólica en las pacientes tratadas con furosemida comparado con los controles, lo cual puede ser la causa de las diferencias de la persistencia de hipertensión entre ambos grupos.
En este estudio se seleccionó un límite de presión arterial de 150 / 110 mm de Hg para considerar la persistencia de la hipertensión. Este ‘blanco’ terapéutico está basado en las sugerencias de mantener la presión arterial sistólica lo más cerca a los niveles ideales 27. Este límite de presión arterial es consistente con diferentes revisiones sobre el tratamiento con drogas antihipertensivas durante el posparto 1.
Hasta el momento, este es uno de los estudios con mayor número de pacientes seleccionadas en los que se analizan tendencias y cambios de varias características clínicas y de laboratorio en preeclámpticas severas tratadas con furosemida. La principal fortaleza del estudio radica en el hecho que se realizó en un hospital que atiende una importante cantidad de embarazadas. Por lo tanto, la población de estudio representa un amplio espectro de la población, lo que limita la posibilidad de sesgo de selección. Una posible limitación del estudio es la posibilidad de sesgo entre los profesionales que realizaron el estudio, quienes podrían haber prestado mayor atención al grupo de pacientes tratadas con furosemida, pero esta no parece ser la razón de las diferencias entre los dos grupos.
Los resultados de la investigación permiten concluir que el uso de furosemida produce disminuciones significativas en los valores promedios de presión arterial sistólica y diastólica, al igual que en la frecuencia de persistencia de hipertensión postparto en preeclámpticas severas, sin afectar los parámetros de laboratorio ni aumentar la frecuencia de efectos adversos. Estos resultados sugieren que las preeclámpticas severas pueden beneficiarse del uso de este tipo de tratamiento.
BIBLIOGRAFÍA
1. Abalos E, Duley L, Steyn DW, Gialdini C. Antihypertensive drug therapy for mild to moderate hypertension during pregnancy. Cochrane Database Syst Rev. 2018; 10: CD002252.
2. Duley L, Meher S, Jones L. Drugs for treatment of very high blood pressure during pregnancy. Cochrane Database Syst Rev. 2013; (7): CD001449
3. Goel A, Maski MR, Bajracharya S, Wenger JB, Zhang D, Salahuddin S, et al. Epidemiology and mechanisms of de novo and persistent hypertension in the postpartum period. Circulation. 2015; 132(18): 1726-33.
4. Walters BN, Thompson ME, Lee A, de Swiet M. Blood pressure in the puerperium. Clin Sci (Lond). 1986; 71(5): 589-94.
5. Wei J, Wang Y, Xu J, Zhang C, Zhou H, Liu G. Clinical study on the factors affecting the post-partum recovery of patients with hypertensive pregnancy disorders at a Chinese hospital. J Obstet Gynaecol Res. 2017; 43(3): 456-461
6. Hussein W, Lafayette RA. Renal function in normal and disordered pregnancy. Curr Opin Nephrol Hypertens. 2014; 23(1): 46-53.
7. Cairns AE, Pealing L, Duffy JMN, Roberts N, Tucker KL, Leeson P, et al. Postpartum management of hypertensive disorders of pregnancy: a systematic review. BMJ Open. 2017; 7(11): e018696.
8. Bernstein PS, Martin JN Jr, Barton JR, Shields LE, Druzin ML, Scavone BM, et al. Consensus bundle on severe hypertension during pregnancy and the postpartum period. J Midwifery Womens Health. 2017; 62(4): 493-501.
9. Saritas T, Moeller MJ. Glomerular disease: pre-eclampsia, podocyturia and the role of parietal epithelial cells. Nat Rev Nephrol. 2014; 10(11): 615-6.
10. Ascarelli MH, Johnson V, McCreary H, Cushman J, May WL, Martin JN Jr. Postpartum preeclampsia management with furosemide: a randomized clinical trial. Obstet Gynecol. 2005; 105(1): 29-33.
11. Dyer RA, Piercy JL, Reed AR, Lombard CJ, Schoeman LK, James MF. Hemodynamic changes associated with spinal anesthesia for cesarean delivery in severe preeclampsia. Anesthesiology. 2008; 108(5): 802-11.
12. Carr DB, Gavrila D, Brateng D, Easterling TR. Maternal hemodynamic changes associated with furosemide treatment. Hypertens Pregnancy. 2007; 26(2): 173-8.
13. Goulopoulou S. Maternal vascular physiology in preeclampsia. Hypertension. 2017; 70(6): 1066-1073.
14. Crozier TM, Wallace EM, Parkin WG. Haemodynamic assessment in pregnancy and pre-eclampsia: A Guytonian approach. Pregnancy Hypertens. 2015; 5(2): 177-81.
15. Rodriguez GC, Albarran HA, Zeron HM. Hemodynamic evaluation and anti-hypertensive schemes used in puerperal women following pre-eclampsia. Mymensingh Med J. 2012; 21(2): 327-32.
16. Risberg A, Sjöquist M, Wedenberg K, Olsson U, Larsson A. Water balance during parturition and early puerperium: A prospective open trial. Clin Biochem. 2015; 48(13-14): 837-42
17. Anthony J, Schoeman LK. Fluid management in pre-eclampsia. Obstet Med. 2013; 6(3): 100-104.
18. Lambert G, Brichant JF, Hartstein G, Bonhomme V, Dewandre PY. Preeclampsia: an update. Acta Anaesthesiol Belg. 2014; 65(4): 137-49.
19. Gandhi S, Sun D, Park AL, Hladunewich M, Silversides CK, Ray JG. The Pulmonary Edema Preeclampsia Evaluation (PEPE) Study. J Obstet Gynaecol Can. 2014; 36(12): 1065-1070.
20. Matthews G, Gornall R, Saunders NJ. A randomized placebo controlled trial of loop diuretics in moderate/severe pre-eclampsia, following delivery. J Obstet Gynaecol. 1997; 17(1): 30-2.
21. Veena P, Perivela L, Raghavan SS. Furosemide in postpartum management of severe preeclampsia: A randomized controlled trial. Hypertens Pregnancy. 2017; 36(1): 84-89.
22. Titze J. Water-free sodium accumulation. Semin Dial. 2009; 22(3): 253-5.
23. Kreepala C, Luangphiphat W, Villarroel A, Kitporntheranunt M, Wattanavaekin K, Piyajarawong T. Effect of magnesium on glomerular filtration rate and recovery of hypertension in women with severe preeclampsia. Nephron. 2018; 138(1): 35-41.
24. Ueda A, Kondoh E, Kawasaki K, Mogami H, Chigusa Y, Konishi I. Magnesium sulphate can prolong pregnancy in patients with severe early-onset preeclampsia. J Matern Fetal Neonatal Med. 2016; 29(19): 3115-20.
25. Goodlin RC. Venous reactivity and pregnancy abnormalities. Acta Obstet Gynecol Scand. 1986; 65(4): 345-8.
26. Valensise H, Vasapollo B, Novelli GP, Pasqualetti P, Galante A, Arduini D. Maternal total vascular resistance and concentric geometry: a key to identify uncomplicated gestational hypertension. BJOG. 2006; 113(9): 1044-52.
27. Shields LE, Wiesner S, Klein C, Pelletreau B, Hedriana HL. Early standardized treatment of critical blood pressure elevations is associated with a reduction in eclampsia and severe maternal morbidity. Am J Obstet Gynecol. 2017; 216(4): 415.e1-415.e5.