2019
4
Autores:
Valentina Fernández Ladrón 1 ,Sara Aguirre Gorospe 1 ,Sonia Lapeña Calavia 1 Orencio Tarrío Fernández 1 ,Juan Carlos Muruzabal Torquemada 1.
Instituciones:
1 Servicio de Ginecología y Obstetricia. Complejo Hospitalario de Navarra-B. Pamplona. Navarra.
Correspondencia:
Valentina Fernández Ladrón
Servicio Ginecología y Obstetricia. Complejo Hospitalario de Navarra.-B. Hospital Virgen del Camino. C/Irunlarrea 4. CP 31008. Navarra. Pamplona. España. Teléfono +34 848422222
e-mail: fernandezvalentina@hotmail.com.
Tipo de documento:
Casos ClínicosSarcoma mieloide uterino como manifestacion de leucemia aguda mieloide
Contenido del documento:
RESUMEN
Introducción y objetivos: El sarcoma mieloide puede ser la primera manifestación de la leucemia mieloide aguda (LMA), presentarse simultáneamente o constituir una forma de recaída.
Material y métodos: Presentamos el caso de una paciente con sarcoma mieloide uterino, como forma de recaída de LMA.
Resultados: El diagnóstico se basa en los hallazgos histopatológicos, la inmunohistoquímica y el inmunofenotipo. El tratamiento y el pronóstico son similares a LMA.
Conclusión: La afectación uterina por leucemia mieloide extramedular es rara pero debe tenerse en cuenta en el diagnostico diferencial de una masa uterina en aquellas pacientes con antecedentes de LMA.
PALABRAS CLAVE: Sarcoma mieloide, leucemia mieloide aguda, inmunohistoquímica. ABSTRACT
Introduction and objectives: Myeloid Sarcoma can present as a first MLA sign, concurrently with or at relapse form.
Materials and methods: We present the case of a patient with uterine myeloid sarcoma, as a form of relapse of MLA.
Results: The diagnostic is based on the histopathology findings along with immunohistochemistry and immunophenotyping.
Conclusion: Uterine involvement due to extramedullary myeloid leukemia is rare but it should be taken into account in the differential diagnosis of a uterine mass in those patients with a history of MLA.
KEYWORDS: Myeloid Sarcoma, acute myeloid leukemia, immunohistochemistry.
INTRODUCCIÓN
El sarcoma mieloide es un tumor extramedular de línea granulocítica que anteriormente se conocía como sarcoma granulocítico, cloroma o tumor leucémico extramedular. Se produce en el 1.5% a 3% de los pacientes con leucemias agudas y en algunos
enfermos con síndromes mielodisplásicos o mieloproliferativos de riesgo alto. Puede ser la primera manifestación de la leucemia mieloide aguda (LMA), presentarse simultáneamente o constituir una forma de recaída. El diagnóstico se basa en los hallazgos histopatológicos, en la inmunohistoquímica y en el inmunofenotipo, permitiendo la clasificación en
REV CHIL OBSTET GINECOL 2019; 84(4): 332 – 336
333
diferentes tipos de sarcomas mieloides con diferentes pronósticos. El diagnóstico diferencial incluye algunos linfomas no Hodgkin de alto grado de malignidad, tumores de células pequeñas redondas, carcinomas indiferenciados y algunas lesiones no malignas. Por lo general el tratamiento y el pronóstico son similares a LMA (1).
El objetivo de esta comunicación es tratar sobre la incidencia, diagnóstico y tratamiento de este proceso, así como realizar una revisión de la literatura existente. Para ello presentamos el caso de una paciente con recaída de LMA en forma de sarcoma uterino.
CASO CLINICO
Mujer de 68 años con antecedentes de Leucemia Mieloide Aguda hace 4 años en remisión tras tratamientos con trasplante de médula alogénico de hermano HLA idéntico (compatible) y Quimioterapia con citarabina e idarubicina.
Cuatro meses antes presentó trombosis en cayado de la vena safena mayor iniciándose tratamiento anticoagulante con Enoxaparina subcutánea a dosis de 1.5 mgr/Kgr cada 24 horas.
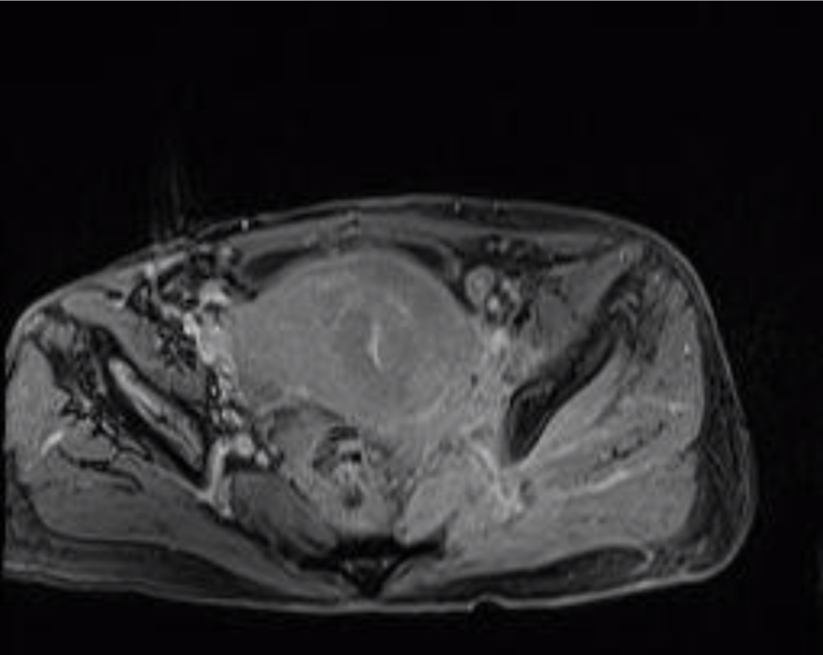
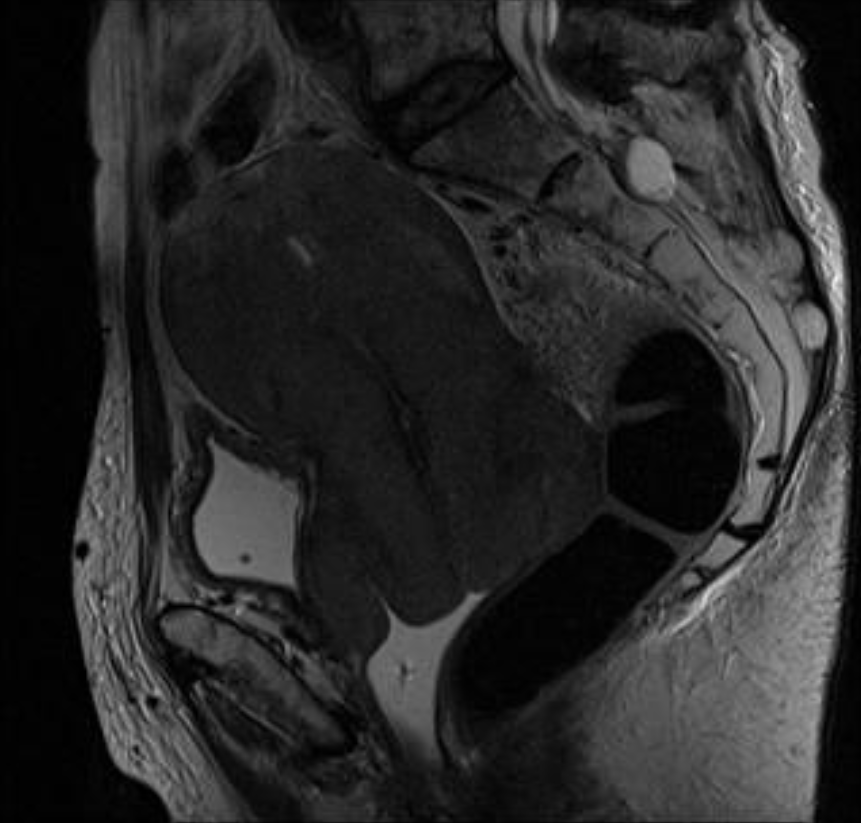
Después de 2 meses se objetivó empeoramiento de la función renal, por lo que se realizó ecografía abdominal que informó de hidronefrosis bilateral grado III. Se colocó catéter doble J en riñón derecho siendo imposible cateterizar el izquierdo. Dentro del estudio etiológico se solicitó resonancia magnética con contraste gadolinio (Figuras 1 y 2) que muestra un tumor comprimiendo el cayado de la safena, aumento de tamaño del cérvix uterino con signos de infiltración tanto craneal como lateral hacia parametrios y pared pélvica, dilatación ureteral bilateral e invasión de musculatura obturadora y glútea. Estos hallazgos sugerían neoplasia cérvix estadio IIIB.
La paciente es derivada a ginecología. En exploración ginecológica destaca cérvix indurado, en tonel, con infiltración vaginal posterior, parametrios borrados y fijos, y alta vascularización con sangrado al mínimo roce.
En ecografía transvaginal se observa cérvix engrosado, muy vascularizado, preservando canal cervical. En fosa ilíaca izquierda, tumor de 47×49 mm, heterogéneo, vascularizado y de bordes irregulares. Se solicitan marcadores tumorales con valores normales (Ca 125:12KU/L, Ca 19.9: 8KU/L y Scc 1.4 mcgr/l).
Se realiza biopsia cervical con resultado de pared vaginal, labio posterior y anterior de cérvix infiltrados por sarcoma mieloide con índice de proliferación Ki-67 del 95%, mitosis aisladas y positividad para CD45, FMPO, CD 34, Bcl-2, CD 99, CD 123, FLi I, P 53. WT- 1, CD10 y p 16 (marcadores para sarcoma y tumores de estirpe mieloide). Ausencia de disrupción del gen EWS (proteína del sarcoma de Ewing).
Se solicita TAC de tórax, abdomen y pelvis con contraste con profilaxis de insuficiencia renal con sueroterapia y acetilcisteina que muestra tumor de cérvix uterino con preservación de cavidad endometrial, dilatación de vías excretoras en ambos riñones y adenopatías menores a un centímetro interaortocava y para-aorticas izquierdas.
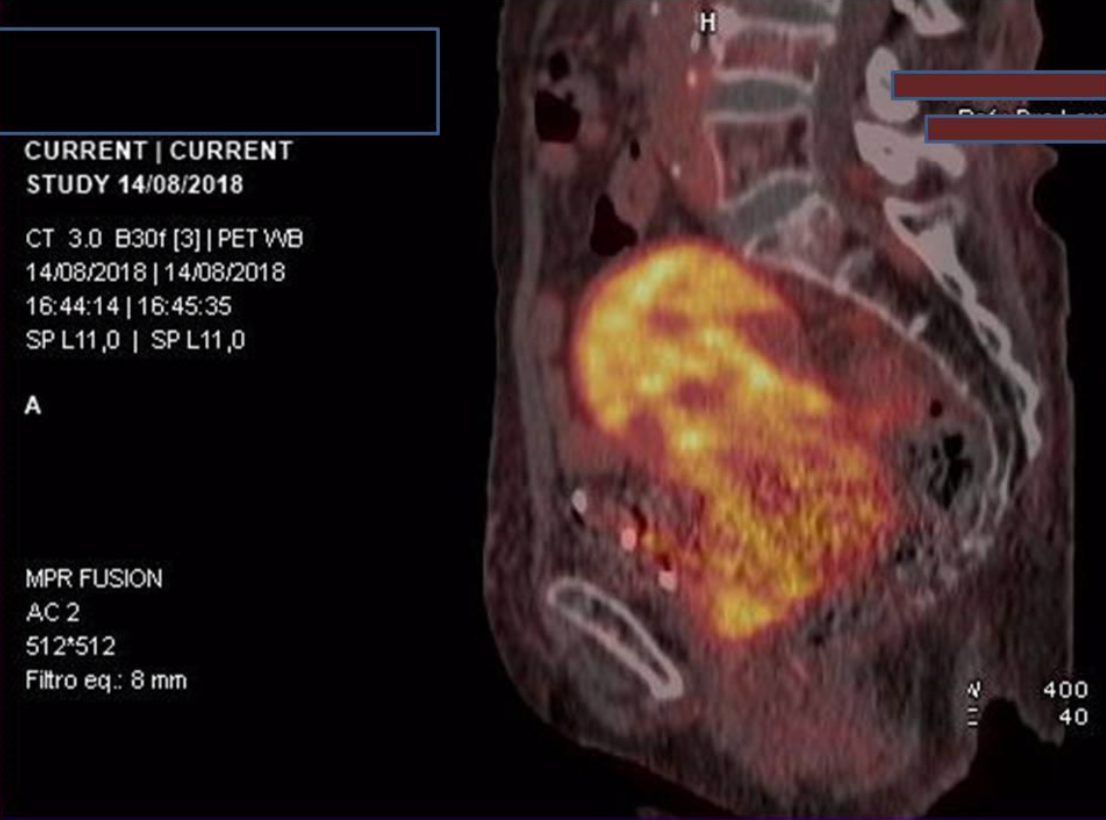
Se completa estudio con PET-TC (Figura 3) que confirma masa pélvica con alta captación (SUVmax =7.7) que infiltra pared anterior y musculatura pélvica, engrosamiento pleural bilateral compatible con enfermedad tumoral ( SUVmax=4,2), así como 2 focos en páncreas (SUVmax=4) y nódulos en médula ósea sugestivos de malignidad (SUVmax=4,2). Captación patológica en mama izquierda ( SUVmax=2,5).
Con los hallazgos radiológicos, histológicos e inmunohistoquímicos y los antecedentes de la paciente se consulta a hematología que considera la existencia de recaída de LMA en forma de sarcoma mieloide, solicitando medulograma (hipocelular con 7% blastos) y citometría (1,8% células CD34+ patológicas) que confirman diagnóstico.
Se inicia quimioterapia según protocolo FLAG-IDA (Fludarabina, Ara-C, Factores estimulantes de colonias e Idarrubicina).
DISCUSIÓN
La leucemia mieloide extramedular (LME) afecta entre el 3 y el 5% de los pacientes con LMA (2,3).Su incidencia es de 0.7/106 en población joven y 2/106 en adultos (4).
Hueso, ganglios linfáticos, piel, tracto gastrointestinal y órbita suelen ser los más afectados. En la población femenina, el tracto genital y la mama se pueden dañar, aunque con menor frecuencia. Dentro del aparato genital de la mujer el órgano más afectado es el ovario, estimado en el 36.4%, seguido del cérvix y útero (5-7). La alteración uterina se suele presentar en la cuarta y quinta décadas de la vida (2-9) aunque la paciente de nuestro caso era mayor.
La presentación clínica del compromiso uterino por LMA puede ser muy diversa. El 82% de los casos se manifiesta como hemorragia uterina anormal, el 29%
REV CHIL OBSTET GINECOL 2019; 84(4): 332 – 336
334
como dolor pélvico y con síntomas sistémicos en el 17.5%, como ocurrió en nuestra paciente, que permanecía asintomática desde el punto de vista ginecológico.
A la exploración física suele ser común hallar una masa en cérvix, o un útero agrandado y poco móvil. Dado que es una entidad que puede presentarse antes, durante o después de presentar una LMA, hay que tenerla en cuenta dentro del diagnóstico diferencial de cualquier masa cervical y/o uterina, incluso a pesar de que el riesgo de recaída disminuye pasados tres años desde la remisión completa. El caso que nos ocupa presentó la enfermedad a los cuatro años.
Los estudios de imagen son útiles, aunque no específicos, y, en la mayoría de los casos, confirman la presencia de un tumor ya detectado o sospechado en el examen físico (2). El PET-TC tiene valor para la detección de focos tempranos, analizando la extensión de la enfermedad y ayudando al planteamiento terapéutico (4).
El diagnóstico inicial puede ser confuso dado que los datos obtenidos en un primer momento sugieren una neoplasia de cérvix, por lo que son esenciales los estudios especiales de inmunohistoquímica para la clasificación correcta. El diagnostico diferencial incluye varios tumores malignos, incluyendo cáncer cervical, tumores neuroendocrinos y linfoma (10) y se lleva a cabo la mayoría de las veces tras determinaciones inmunohistoquímicas. Las traslocaciones del gen EWS se encuentran en tumores de tejidos blancos como tumores de Ewing, tumores neuroectodérmicos, tumores de Askin, sarcoma de células claras, melanoma maligno de tejidos blandos, liposarcoma y condrosarcoma mixoide. Al no objetivarse disrupciones en este gen es posible descartar estos tipos de tumores. El resto de marcadores más específicos de sarcoma y de línea mieloide resultan positivos, haciendo de la inmunohistoquímica una pieza clave en el diagnostico. Posteriormente los estudios de medulograma y citometría confirman el diagnóstico y determinan el grado de maduración y de diferenciación de las células implicadas.
La quimioterapia sistémica es la piedra angular del tratamiento, aunque el pronóstico no es bueno relacionándose con la evolución de la LMA, con una supervivencia descrita de entre 7 meses y 2 años (3,8- 9,11-14). No se planteó tratamiento quirúrgico ni local del tumor en primera instancia debido a la infiltración de tejidos adyacentes, al compromiso ureteral y a la
presencia de enfermedad a distancia. El papel de la radioterapia sigue siendo controvertido (5).
En la literatura existen casos publicados similares al de nuestra paciente de LMA cervical después de remisión (5, 9,15) aunque de momento son casos aislados o series pequeñas y es difícil establecer conclusiones.
CONCLUSIONES
Aunque la afectación uterina por leucemia mieloide extramedular sea rara y no existan muchos casos reportados al respecto, es una entidad a tener en cuenta en el diagnostico diferencial de una masa uterina en aquellas pacientes con antecedentes de LMA.
Pero también habrá que sospecharla en el resto de las mujeres ya que puede ser la primera manifestación ó presentarse de forma simultánea a la misma.
Bibliografia
1-. Lombardi V, Pedrini F, Casas G, Riveros D, Stengel FM. Sarcoma mieloide: presentación cutánea de novo. Arch. Argent. Dermatol.2013;63:13-16.
2. Breccia M, Mandelli F, Petti MC, D`Andrea M, Pescarmona E, Pileri SA, et al. Clinico-pathological characteristics of myeloid sarcoma at diagnosis and during follow-up: report of 12 cases from a single institution. Leuk Res.2004;28:1165-9.
3. Friedman HD, Adelson MD, Elder RC, Lemke SM. Granulocytic sarcoma of the uterine cervix – literature review of granulocytic sarcoma of the female genital tract. Gynecol Oncol.1992;46:128-37.
4-.GuiW,LiJ,ZhangZ,WangL,ZhaoJ,MaL,SuL. Primary hematological malignancy of the uterine cervix: A case report. Oncol Lett.2019;18(3):3337- 3341.
5-. Chiang YC, Chen CH. Cervical granulocytic sarcoma: report of one case and review of the literature. Eur J Gynaecol Oncol.2010;31(6):697-700.
6-. García-Soto G, Pachón-Rincón JJ, Castaño JA,Torres JD, Gómez EI.Leucemia mieloide extramedular con compromiso endometrial: reporte de un caso y revisión de la literatura. Rev Colombiana Obstetricia y Ginecologia.2007;58(3):243-248.
REV CHIL OBSTET GINECOL 2019; 84(4): 332 – 336
335
7-.Modi G, Madabhavi I, Panchal H, et al. Primary vaginal myeloid sarcoma: a rare case report and review of the literature. Case Rep Obstet Gynecol. 2015;2015:957490.
8 -.Byrd JC, Edenfield WJ, Shields DJ, Dawson NA. Extramedu l lar y myeloidcel l t u mors in acutenonlymphocyticleukemia: a clinicalreview. J Clin Oncol. 1995;13:1800-16.
9-. Lee JW, Kim YT, Min YH, Kim JW, Kim SH, Park KH, et al. Granulocytic sarcoma of the uterine cervix. Int J Gynecol Cancer.2004;14:553-7.
10-. Yamane A, Sekine T, Machida T, Omori I, Onda M, Kumita S. Imaging findings of solitariy uterine granulocytic sarcoma. Acta Radiologica Open.2017; 6(3): 1-4.
11-. Bennett JM, Catovsky D, Daniel MT, Flandrin G, Galton DA, Gralnick HR, et al. Proposals for the classification of the acute leukaemias. French- American-British (FAB) cooperative group. Br JHaematol.1976;33:451-8.
12-.Jaffe ES, Harris NL, Stein H, Vardiman J W, eds. World Health Organization classification of tumours. Pathology and genetics of tumours of haematopoietic and lymphoid tissues. Lyon, France: IARC Press;2001.
13-.Pathak B, Bruchim I, Brisson ML, HammoudaW, Bloom C, Gotlieb WH. Granulocytic sarcomapresenting as tumors of the cervix. Gynecol Oncol.2005;98:493-7.
14-.Oliva E, Ferry JA, Young RH, Prat J, Srigley JR, Scully RE. Granulocytic sarcoma of the female genital tract: a clinicopathologic study of 11 cases. Am J Surg Pathol.1997;21:1156-65.
15-. Kim SC, Natarajan-Ame S, Lioure B, Chenard MP, Duclos B, Herbrecht R, Bergerat JP. Successful treatment of a granulocytic sarcoma of the uterine cervix in complete remission at six-year follow-up. J Oncol.2010;2010:812424